��Ŀ����
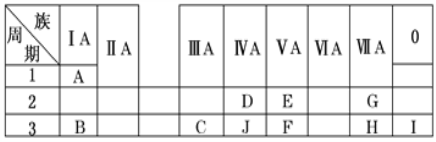
����Ŀ����֪�ɶ����ڳ���Ԫ���γɵĴ�����A��B��C��Dת����ϵ��ͼ1���£�����A������B֮��ķ�Ӧ������Һ�н��У� 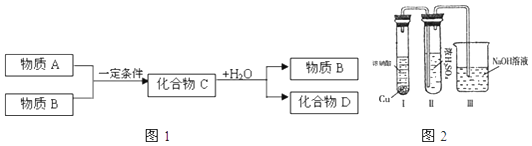
��1����AΪ�������ʣ�C�ǵ���ɫ���壬D��һԪǿ� ������B�����ѧʽ����
�ڻ�����C�ĵ���ʽΪ��������D��������ѧ���������� ��
���ڳ����£���pH=a�Ĵ�����Һ�м�������pH=b��D��Һ����a+b=14�����ַ�Ӧ��������Һ�и������ӵ�Ũ���ɴ�С��˳���ǣ� ��
��2����AΪ�ǽ������ʣ�C����ɫ���壬D��һԪǿ�ᣮ ��BΪ���ѧʽ����
�ڻ�����C��H2O��Ӧ��ѧ����ʽ �� �������뻹ԭ����������Ϊ ��
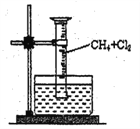
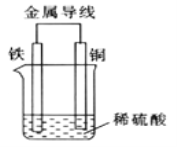
��3��ijͬѧ��ͼ2װ������й�̽��ʵ�飮 ���Թ��з�����Ӧ�����ӷ���ʽΪ ��
���Թ��й۲쵽��ʵ������ʱ��˵��NO2������Ũ�����У�Ũ����ܸ���NO2 ��
���𰸡�
��1��O2�� ![]() �����ۼ������Ӽ��� c��CH3COO������c��Na+����c��H+����c��OH����
�����ۼ������Ӽ��� c��CH3COO������c��Na+����c��H+����c��OH����
��2��NO��3NO2+H2O�T2HNO3+NO��1��2
��3��Cu+4H++2NO3��=Cu2++2NO2��+2H2O��ŨH2SO4��δ�����������ݳ�,��ŨH2SO4����ɫ��Ϊ����ɫ��֤��NO2������Ũ�����У�
���������⣺��1����AΪ�������ʣ�C�ǵ���ɫ���壬ӦΪNa2O2����AΪNa��D��һԪǿ�ӦΪNaOH����
��AΪNa��C�ǵ���ɫ���壬ӦΪNa2O2����BΪO2�����Դ��ǣ�O2��
��CΪNa2O2��Ϊ���ӻ�����Ϊ������ʽΪ ![]() ��DΪNaOH�����й��ۼ������Ӽ������Դ��ǣ�
��DΪNaOH�����й��ۼ������Ӽ������Դ��ǣ� ![]() �����ۼ������Ӽ���
�����ۼ������Ӽ���
�����ڳ����£���pH=a�Ĵ�����Һ�м�������pH=b��NaOH��Һ����a+b=14������ 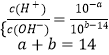 ��
��
��֮�ã�c��H+��=c��OH������������Ϊ���ᣬ������������Ӧ����Һ�����ԣ�
����c��CH3COO������c��Na+����c��H+����c��OH������c��Na+����c��H+����
����c��CH3COO������c��Na+����c��H+����c��OH������
���Դ��ǣ�c��CH3COO������c��Na+����c��H+����c��OH��������2��C����ɫ���壬ӦΪNO2��AΪ�ǽ������ʣ�ӦΪO2����BΪNO��DΪHNO3��
�������Ϸ�����֪BΪNO�����Դ��ǣ�NO��
��NO2��ˮ��Ӧ����HNO3��NO����Ӧ�ķ���ʽΪ3NO2+H2O=2HNO3+NO���ɷ���ʽ��֪�������뻹ԭ����������Ϊ 1��2��
���Դ��ǣ�3 NO2+H2O�T2 HNO3+NO�� 1��2����3��Ũ������ͭ��Ӧ��������ͭ�Ͷ�����������Ӧ�����ӷ���ʽΪCu+4H++2NO3��=Cu2++2NO2��+2H2O����NO2������Ũ�����У���ŨH2SO4��δ�����������ݳ�������Һ�ʺ���ɫ��
���Դ��ǣ�Cu+4H++2NO3��=Cu2++2NO2��+2H2O��ŨH2SO4��δ�����������ݳ�����ŨH2SO4����ɫ��Ϊ����ɫ��֤��NO2������Ũ�����У���

 ���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�����Ŀ���й���ͳ�Ļ��������������Ŵ������г�ּ����˹Ŵ���ѧ�о��ɹ������й���KNO3�ĹŴ����ף�����˵������������
Ŀ�� | �Ŵ����� | ˵�� | |
A | ���� | ����������(KNO3)����������ʯ�ʣ��༤�����������ɲ⡱һ���칤��� | KNO3����ȼ |
B | ���� | ������ʯ(KNO3)������(Na2SO4):���Ի���֮����������������ʯҲ�� ���������ݾ���ע�� | ������ɫ��Ӧ |
C | �ᴿ | ����(KNO3)����ɽ���µ�����˪��ɨȡ��ˮ��֭���˼������ɡ��������������ݡ� | �ܽ⡢�������ᾧ |
D | ʹ�� | ��(��ҩ)������(KNO3)����ǡ�ɽľ̿���ϣ���Ϊ����ͭ��ҩ��"���������ݸ�Ŀ�� | ����KNO3�������� |
A. A B. B C. C D. D