题目内容
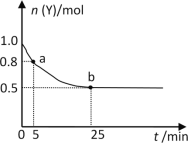
【题目】恒温时,向2L密闭容器中通入一定量的气体X和Y,发生反应:3X(g)+Y(g)![]() 2Z(g) ΔH>0。Y的物质的量n(Y)随时间t变化的曲线如图所示。下列说法正确的是( )
2Z(g) ΔH>0。Y的物质的量n(Y)随时间t变化的曲线如图所示。下列说法正确的是( )
A.该反应为放热反应
B.0~5min内,以X表示的化学反应速率是0.02mol·L-1·min-1
C.b点时该反应达到了最大限度,反应停止
D.25min时,c(Z)=0.5mol·L-1
【答案】D
【解析】
A.由于△H>0,该反应属于吸热反应,故A错误;
B.0~5min内,由图像可知△n(Y)=1mol-0.8mol=0.2mol,则根据3X(g)+Y(g)![]() 2Z(g)可求出△n(X)=0.2mol×3=0.6mol,以X表示的化学反应速率是v(X)=
2Z(g)可求出△n(X)=0.2mol×3=0.6mol,以X表示的化学反应速率是v(X)=  =0.06mol·L-1·min-1,故B错误;
=0.06mol·L-1·min-1,故B错误;
C.b点时该反应达到了最大限度,某一组分的消耗速率与生成速率相等,反应没有停止,故C错误;
D.25min时,由图像可知△n(Y)=1mol-0.5mol=0.5mol,则根据3X(g)+Y(g)![]() 2Z(g)可求出△n(Z)=0.5mol×2=1.0mol,c(Z)=
2Z(g)可求出△n(Z)=0.5mol×2=1.0mol,c(Z)= ![]() =0.5mol/L;故D正确;
=0.5mol/L;故D正确;
答案为D。

 阅读快车系列答案
阅读快车系列答案【题目】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1)今有如下两个热化学方程式:则a _____ b (填“>”、“=”或“<”)
H2(g)+![]() O2(g)═H2O (l) △H1=a kJmol﹣1
O2(g)═H2O (l) △H1=a kJmol﹣1
H2(g)+![]() O2(g)═H2O (g) △H2=b kJmol﹣1
O2(g)═H2O (g) △H2=b kJmol﹣1
(2)拆开lmol气态物质中某种共价键需要吸收的能量叫键能,部分化学键键能如表。
化学键 | H﹣H | N﹣H | N≡N |
键能/kJmol﹣1 | 436 | a | 945 |
已知反应N2(g)+3H2(g)=2NH3(g) △H=-93 kJmol﹣1,试根据表中所列键能数据计算a=______________。
(3)利用水煤气合成二甲醚(CH3OCH3)的三步反应如下:
①2H2(g)+ CO(g)═ CH3OH(g) △H1
②2CH3OH(g)═ CH3OCH3(g)+ H2O(g) △H2
③3 H2(g)+3CO(g)═ CO2(g) + CH3OCH3(g) △H3
反应③为制取二甲醚的第3步反应,利用△H1和△H2计算△H3时,还需要利用________反应的△H。
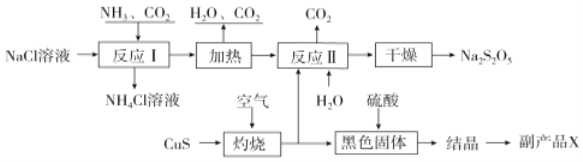
(4)中科院大连化学物理研究所的科研人员在新型纳米催化剂Na-Fe3O4和HMCM-22 的表面将CO2转化为烷烃,其过程如图。
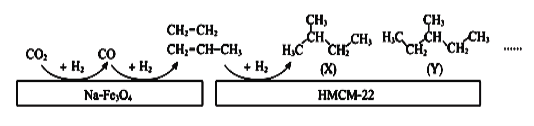
图中CO2转化为CO的反应为: CO2(g)+H2(g) = CO(g)+H2O(g) △H= +41kJ/mol
已知:2CO2(g) + 6H2(g) = C2H4(g) + 4H2O(g) △H= -128kJ/mol
则图中CO转化为C2H4的热化学方程式是______________________________________。
【题目】对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ(pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ(pH=4,含Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是
A. 在0~20min内,I中M的分解速率为0.015 mol·L-1·min-1
p>B. 水样酸性越强,M的分解速率越快C. 在0~25min内,III中M的分解百分率比II大
D. 由于Cu2+存在,IV中M的分解速率比I快