题目内容
(5分)用VSEPR模型和杂化轨道理论相关知识填表:
| 分子或离子 | 孤对电子对数 | VSEPR模型名称 | 中心原子杂化轨道类型 | 分子或离子的立体构型名称 |
| CH4 | 0 | 正四面体形 | sp3 | 正四面体形 |
| BeCl2 | | | | |
| SO2 | | | | |
| CH3+ | | | | |
| SO42- | | | | |
| NCl3 | | | | |
(5分)
| 分子或离子 | 孤对电子对数 | VSEPR模型名称 | 中心原子杂化轨道类型 | 分子或离子的立体构型名称 |
| CH4 | 0 | 正四面体形 | sp3 | 正四面体形 |
| BeCl2 | 0 | 直线型 | sp | 直线型 |
| SO2 | 1 | 平面三角形 | sp2 | V形 |
| CH3+ | 0 | 平面三角形 | sp2 | 平面三角形 |
| SO42- | 0 | 正四面体形 | sp3 | 正四面体形 |
| NCl3 | 1 | 四面体形 | sp3 | 三角锥形 |
根据价层电子对互斥理论可知,甲烷知碳原子含有的孤对电子对数是(4-1×4)÷2=0,所以甲烷分子的构型是正四面体形,其中碳原子是sp3杂化。BeCl2中Be原子含有的孤对电子对数是(2-1×2)÷2=0,因此是直线型结构,属于sp杂化。SO2中硫原子含有的孤对电子对数是(6-2×2)÷2=1,则SO2是V形结构,是sp2杂化。CH3+中碳原子含有的孤对电子对数是(4―1―1×3)÷2=0,因此是平面三角形结构,属于sp2杂化。SO42-中硫原子含有的孤对电子对数是(6+2-2×4)÷2=0,所以是正四面体形,属于sp3杂化。NCl3中氮原子含有的孤对电子对数是(5-1×3)÷2=1,因此结构是三角锥形,属于sp3杂化

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目

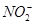

 ②
② 、③
、③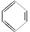 、④ HCHO等,其中碳原子采取sp2杂化的分子有________(填序号);HCHO分子的空间构型为________ 。
、④ HCHO等,其中碳原子采取sp2杂化的分子有________(填序号);HCHO分子的空间构型为________ 。