题目内容
10.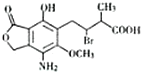 某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为( )
某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为( )| A. | 1:1:1 | B. | 2:4:1 | C. | 1:2:1 | D. | 1:2:2 |
分析 能与Na反应的官能团有羟基、羧基,能与NaOH反应的官能团有酯基、酚羟基、溴原子和羧基,能与碳酸氢钠反应的官能团只有羧基,以此解答.
解答 解:能与Na反应的官能团有羟基、羧基,1mol有机物可消耗2molNa,能与NaOH反应的官能团有酯基、酚羟基、溴原子和羧基,1mol有机物可消耗4molNaOH,能与碳酸氢钠反应的官能团只有羧基,1mol有机物只能消耗1mol碳酸氢钠,消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为2:4:1,
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系解答的关键,侧重羧酸、酯、酚性质的考查,注意水解生成酚的性质为易错点,题目难度不大.

练习册系列答案
相关题目
1.4NH3+5O2≒4NO+6H2O反应在5L的密闭容器中进行,半分钟后,NO物质的量增加了0.3mol,则此反应的反应速率为( )
| A. | V(O2)=0.01mol/L•s | B. | V(NO)=0.008mol/L•s | ||
| C. | V(H2O)=0.003mol/L•min | D. | V(NH3)=0.002mol/L•s |
18.用下列气体和溶液进行喷泉实验,最终液体不能充满烧瓶的是( )
| A. | CO2和NaOH溶液 | B. | NO2和水 | C. | NH3和水 | D. | Cl2和NaOH溶液 |
2.下列实验方案的设计、结论正确的是( )
| A. | 用 NaHCO3 溶液可一次鉴别出稀盐酸、NaOH溶液、AlCl3溶液、NaAlO2 溶液 | |
| B. | 高锰酸钾试剂瓶内壁上黑色物质可用稀盐酸洗涤 | |
| C. | 除去SO2 中少量HCl,将其通入饱和的Na2SO3 溶液 | |
| D. | 将硝酸铵晶体溶于水,测得水温下降,证明硝酸铵水解是吸热的 |
10.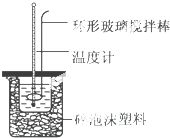 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据
完成下列问题
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是Cu传热快,热量损失大.
(2)在操作正确的前提下,提高中和热测定准确性的关键是提高装置的保温效果.
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=-56.8 kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].如果用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将偏大(填“偏大”、“偏小”或“不变”).
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是ABE.
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大.
 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据| 实验次数 | 起始温度t1/℃ | 终止温 度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是Cu传热快,热量损失大.
(2)在操作正确的前提下,提高中和热测定准确性的关键是提高装置的保温效果.
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=-56.8 kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].如果用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将偏大(填“偏大”、“偏小”或“不变”).
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是ABE.
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大.
11.水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C(s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
(1)该反应的平衡常数K随温度的升高而增大(增大、减小、不变).
(2)上述反应达到平衡后,增加H2O(g)的量,则C(s)的物质的量减小(增大、减小、不变).
(3)下列说法一定能判断如上反应达平衡的是BD
A.消耗1mol H2O(g)同时生成1mol H2
B.容器内混合气体的总质量不变
C.H2O(g)、CO (g)、H2 (g)三种气体的浓度比为1:1:1
D.恒温恒容时容器内气体的压强不变
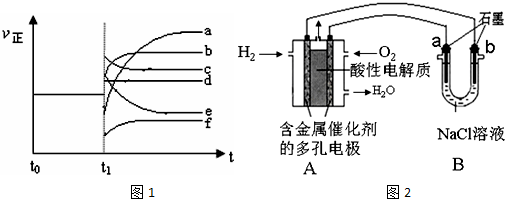
(4)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如图1所示,
填出对应的编号.
①缩小容器体积b;
②降低温度f;
(5)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中①②相应的空格.
(6 )如图2是利用氢氧燃料作电源,用惰性电极电解200ml 1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气4.48L(设电解后溶液体积不变).
①电解后溶液的pH=14(忽略氯气与氢氧化钠溶液反应)
②阳极产生气体的体积在标准状况下是3.36 L.

C(s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
(1)该反应的平衡常数K随温度的升高而增大(增大、减小、不变).
(2)上述反应达到平衡后,增加H2O(g)的量,则C(s)的物质的量减小(增大、减小、不变).
(3)下列说法一定能判断如上反应达平衡的是BD
A.消耗1mol H2O(g)同时生成1mol H2
B.容器内混合气体的总质量不变
C.H2O(g)、CO (g)、H2 (g)三种气体的浓度比为1:1:1
D.恒温恒容时容器内气体的压强不变
(4)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如图1所示,
填出对应的编号.
①缩小容器体积b;
②降低温度f;
(5)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中①②相应的空格.
| 容器编号 | c(H2O)/mol•L-1 | c(CO)/mol•L-1 | c(H2)/mol•L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ①0.6 | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ②ν正>ν逆 |
①电解后溶液的pH=14(忽略氯气与氢氧化钠溶液反应)
②阳极产生气体的体积在标准状况下是3.36 L.
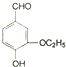 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.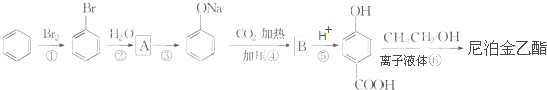
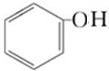 ,B
,B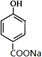 ;
;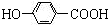 +CH3CH2OH$→_{△}^{离子液体}$
+CH3CH2OH$→_{△}^{离子液体}$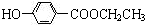 +H2O.
+H2O. .
.