题目内容
18.用下列气体和溶液进行喷泉实验,最终液体不能充满烧瓶的是( )| A. | CO2和NaOH溶液 | B. | NO2和水 | C. | NH3和水 | D. | Cl2和NaOH溶液 |
分析 进行喷泉实验,最终液体不能充满烧瓶,说明气体不能被溶液全部吸收,结合气体和溶液的性质判断.
解答 解:A.氢氧化钠足量,二氧化碳可全部被吸收生成碳酸钠溶液,进行喷泉实验,最终液体能充满烧瓶,故A不选;
B.二氧化氮与水反应生成硝酸和NO,NO不溶于水,不能充满烧瓶,故B选;
C.氨气极易溶于水,氨气能够全部被水吸收,进行喷泉实验,最终液体能充满烧瓶,故C不选;
D.氢氧化钠足量,氯气可全部被吸收生成氯化钠、次氯酸钠溶液,进行喷泉实验,最终液体能充满烧瓶,故D不选;
故选:B.
点评 本题考查常见气体的性质以及喷泉实验,明确喷泉实验原理是关键,注意各种气体的性质,题目难度不大.

练习册系列答案
相关题目
8.为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施.化学反应的反应热通常用实验进行测定,也可进行理论推算.
(1)25℃下实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452.8KJ/mol
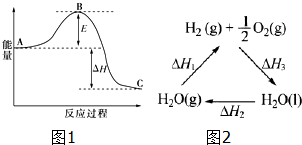
(2)合成氨反应:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g),反应过程的能量变化如图1所示.已知N2(g)与H2(g)反应生成34gNH3(g),放出92.2kJ的热量.请回答下列问题:
该反应通常用铁作催化剂,加催化剂会使图中E变小(填“大”或“小”),图中△H=-46.1kJ/mol
(3)由气态基态原子形成1mol化学键释放的能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.
已知反应N2(g)+3H2(g)═2NH3(g)△H=a kJ•mol-1.试根据表中所列键能数据估算a 的值:-93.
(4)已知:△H2=+44kJ•mol-1,△H3=-285.8kJ•mol-1图2列出它们之间的转变关系.请计算298K时由H2O(g)生成1molH2(g)和1/2molO2(g)反应的△H1=-(△H2+△H3)(用△H2、△H3表示△H1计算等式),+241.8kJ•mol-1(计算△H1数据结果).
(1)25℃下实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452.8KJ/mol
(2)合成氨反应:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g),反应过程的能量变化如图1所示.已知N2(g)与H2(g)反应生成34gNH3(g),放出92.2kJ的热量.请回答下列问题:
该反应通常用铁作催化剂,加催化剂会使图中E变小(填“大”或“小”),图中△H=-46.1kJ/mol
(3)由气态基态原子形成1mol化学键释放的能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
(4)已知:△H2=+44kJ•mol-1,△H3=-285.8kJ•mol-1图2列出它们之间的转变关系.请计算298K时由H2O(g)生成1molH2(g)和1/2molO2(g)反应的△H1=-(△H2+△H3)(用△H2、△H3表示△H1计算等式),+241.8kJ•mol-1(计算△H1数据结果).

9.既不能用浓硫酸干燥,又不能用碱石灰干燥的是( )
| A. | NH3 | B. | H2S | C. | SO2 | D. | HCl |
6.为除去括号内的杂质,下列各选项中所选用的试剂或方法不正确的是( )
| A. | NaHCO3溶液(Na2CO3),应通入过量的CO2气体 | |
| B. | NaBr溶液(NaI),应加入适量的氯水、CCl4,进行萃取分液 | |
| C. | NH4Cl溶液(FeCl3),应加入适量的氨水,过滤 | |
| D. | CO2(CO),通过过量的灼热的氧化铜粉末 |
3. 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )
 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )| A. | 1mo N2(g)和1mo O2(g)完全反应放出的能量为180kJ | |
| B. | 通常情况下,N2(g)和O2(g)混合能直接生成NO | |
| C. | 1mol N2(g)和1molO2(g)具有的总能量小于2molN(g)具有的总能量 | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
10.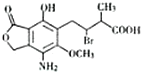 某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为( )
某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为( )
 某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为( )
某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为( )| A. | 1:1:1 | B. | 2:4:1 | C. | 1:2:1 | D. | 1:2:2 |
7.化学与社会、生活密切相关,下列现象或事实与对应的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 蔗糖、淀粉、纤维素等有甜味 | 人体内,糖类在淀粉酶的作用下能发生水解,生成葡萄糖 |
| B | 煤通过气化和液化等化学变化可以有效地控制酸雨 | 煤通过气化和液化处理,其产品中硫的含量将大大降低 |
| C | 地沟油经过处理加工后可用作飞机、汽车燃油 | 地沟油的成分是液态烃 |
| D | 在钢铁制品的表面镀上一层锡,可有效防止其被腐蚀 | 形成原电池时锡是负极被氧化,而钢铁制品作为正极被保护 |
| A. | A | B. | B | C. | C | D. | D |

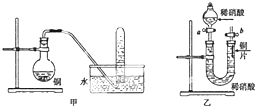 如图是甲、乙两位同学探究铜与稀硝酸.反应还原产物的实验装置图,请回答下列问题:
如图是甲、乙两位同学探究铜与稀硝酸.反应还原产物的实验装置图,请回答下列问题: