题目内容
【题目】下列四种粒子中,半径按由大到小顺序排列的是( )
①基态X的原子结构示意图为
②基态Y的价电子排布式为![]()
③基态Z2-的轨道表示式为![]()
④基态原子W有2个电子层,电子式为![]()
A.![]() B.
B.![]()
C.![]() D.
D.![]()
【答案】C
【解析】
X为S原子,Y为Cl原子,Z2-为S2-,W为F原子,电子层数越多,半径越大,同周期随原子序数增大,原子半径减小,同种元素的阴离子的半径大于原子半径;
①基态X的原子结构示意图: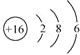 ,则X为S原子,②基态Y的价电子排布式:3s23p5,则Y为Cl原子,③基态Z2-的电子排布图:
,则X为S原子,②基态Y的价电子排布式:3s23p5,则Y为Cl原子,③基态Z2-的电子排布图:![]() ,Z2-为S2-,④W基态原子有2个能层,结合电子式可知,W为F原子;电子层数越多,半径越大,F<Cl,同周期随原子序数增大,原子半径减小,则半径:S>Cl,同种元素的阴离子的半径大于原子半径,则半径:S<S2-;
,Z2-为S2-,④W基态原子有2个能层,结合电子式可知,W为F原子;电子层数越多,半径越大,F<Cl,同周期随原子序数增大,原子半径减小,则半径:S>Cl,同种元素的阴离子的半径大于原子半径,则半径:S<S2-;
所以半径:S2->S>Cl>F,故选:C。
答案选C。

【题目】利用如图装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.25mol·L-1硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55mol·L-1NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ·mol-1)___________。
(2)倒入NaOH溶液的正确操作是__________(从下列选项中选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是________(从下列选项中选出)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的空白:
起始温度t1℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | _____ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55mol·L-1NaOH溶液和0.25mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。则中和热ΔH=________(取小数点后一位)。
【题目】处理、回收利用CO是环境科学家研究的热点课题。回答下列问题:
Ⅰ.处理大气污染物
CO用于处理大气污染物N2O所发生的反应原理为:![]()
![]() 有人提出上述反应可以用“Fe+”作催化剂。
有人提出上述反应可以用“Fe+”作催化剂。
其总反应分两步进行:(1)第一步:![]() ;第二步:____ (写反应方程式)。
;第二步:____ (写反应方程式)。
(2)第二步反应不影响总反应达到平衡所用时间,由此推知,第二步反应速率____ 第一步反应速率(填“大于”“小于”或“等于”)。
Ⅱ.合成天然气(SNG)涉及的主要反应原理如下:
CO甲烷化: ![]()
![]()
水煤气变换: ![]()
![]()
(3)反应![]() 的△H= ___kJ/mol。
的△H= ___kJ/mol。
(4)在一恒容容器中,按照nmolCO和3nmolH2投料发生CO甲烷化反应,测得CO在不同温度下的平衡转化率与压强的关系如右图所示,下列说法正确的是_____(填标号)。

a.温度:T1<T2<T3
b.正反应速率:v(e)>v(c)>v(b)
c.平衡常数:K(a)<K(d)<K(c)
d.平均摩尔质量:M(a)>M(b)=M(e)
(5)在恒压管道反应器中,按n(H2)︰n(CO)=3︰1通入原料气发生CO甲烷化反应,400℃、P总为100kPa时反应体系平衡组成如下表所示。
组分 | H2 | CO | CH4 | H2O | CO2 |
体积分数 | 8.50 | 1.50 | 45.0 | 44.0 | 1.00 |
则该条件下CO的总转化率α= ___。 (保留一位小数)
(6)将制备的CH4用来组成下图所示燃料电池电解制备N2O5

①阳极的电极反应为_____。
②理论上制备1molN2O5,石墨2电极消耗气体的体积为_____L(标准状况)。
【题目】某些共价键的键长数据如下表所示。试根据下表回答问题。
共价键 |
|
|
|
|
|
|
|
|
键长 | 0.154 | 0.134 | 0.121 | 0.143 | 0.123 | 0.146 | 0.122 | 0.110 |
(1)根据表中有关数据,你能推断出影响共价键键长的因素主要有哪些?_______。其影响的结果怎样?__________。
(2)通常,键能越__________,共价键越____,由该键构成的分子越稳定。