题目内容
【题目】磁性材料A由两种元素组成,为探究其组成和性质,设计并完成如下实验:

(1) A的化学式为_____________________________________________________。
(2)用化学方程式表示气体C与氯水反应生成D的过程:___________________________________。
(3)B溶于盐酸后生成的物质F可用于净水,结合离子方程式说明其原因:__________________________。
【答案】 Fe3S4 Cl2+SO2+2H2O===H2SO4+2HCl Fe3++3H2O![]() Fe(OH)3+3H+
Fe(OH)3+3H+
【解析】本题考查以磁性材料为载体考查无机推断题。无色气体C与足量的氯气反应得到溶液D,D中加入氯化钡溶液和盐酸溶液,有白色沉淀E生成,故E为BaSO4,D为硫酸和盐酸的混合液,C为二氧化硫。B溶于盐酸后生成的物质F可用于净水,再结合其A由两种元素组成的磁性材料,可知,B为三氧化铁。(1)氧化铁的质量为2.400g,其物质的量为2.400/160=0.015mol,含铁原子的物质的量为0.030mol,则铁的质量为0.030×56=1.680g,则化合物中硫元素的质量为2.960-1.680=1.280g,硫的物质的量为1.280/32=0.040mol,则铁与硫的物质的量比为0.030:0.040=3:4,则化学式为:Fe3S4;(2)二氧化硫与氯气反应的化学方程式为:Cl2+SO2+2H2O===H2SO4+2HCl;(3) B溶于盐酸后生成的物质F可用于净水即为三价铁离子水解:Fe3++3H2O![]() Fe(OH)3+3H+。
Fe(OH)3+3H+。

 名题金卷系列答案
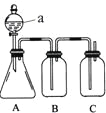
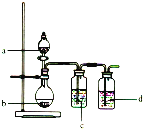
名题金卷系列答案【题目】用如图所示装置制取表中的四种干燥、纯净的气体![]() 图中加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂。上述方法中可以得到干燥、纯净的气体是( )
图中加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂。上述方法中可以得到干燥、纯净的气体是( )
气体 | a | b | c | d |
| 稀盐酸 |
| 饱和 | 浓 |
| 浓盐酸 |
| NaOH溶液 | 浓 |
| 稀 | Cu | 品红溶液浓 |
|
| 稀盐酸 | 锌粒 | NaOH溶液 | 浓 |
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()