题目内容
【题目】W、X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;W是形成有机物种类最多的元素;R2+的3d轨道中有9个电子。请回答:
(1)Y基态原子的电子排布式是__;Y和W形成的三原子分子是__(填“极性”或“非极性”)分子.
(2)X与氢元素可形成的化合物XH3的中心原子杂化轨道类型为___杂化,XH3的立体构型是___。
(3)Z所在周期中第一电离能最大的主族元素Q名称__。比较沸点高低:XY2__ZY。
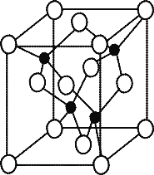
(4)Z与某元素形成的化合物的晶胞如图1所示,晶胞中阴离子与阳离子的个数比是____。

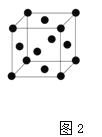
(5)R晶胞结构如图2所示,R晶体中每个R原子周围距离最近的R原子数目为___。
【答案】1s22s22p4 非极性 sp3 三角锥形 氯元素 < 2:1 12
【解析】
W、X、Y、Z、R为前四周期元素,且原子序数依次增大,![]() 是红棕色气体,为
是红棕色气体,为![]() ,则X是N、Y是O元素;X与氢元素可形成
,则X是N、Y是O元素;X与氢元素可形成![]() ;Z基态原子的M层与K层电子数相等,则Z为Mg元素;W是形成有机物种类最多的元素,为C元素;
;Z基态原子的M层与K层电子数相等,则Z为Mg元素;W是形成有机物种类最多的元素,为C元素;![]() 的3d轨道中有9个电子,则R原子核外电子数
的3d轨道中有9个电子,则R原子核外电子数![]() ,为Cu元素。
,为Cu元素。
(1)![]() 为O元素,其基态原子核外有8个电子,根据构造原理书写O基态原子的电子排布式为
为O元素,其基态原子核外有8个电子,根据构造原理书写O基态原子的电子排布式为![]() ;中心重合的分子为非极性分子,不重合的分子为极性分子,Y和W形成的三原子分子为
;中心重合的分子为非极性分子,不重合的分子为极性分子,Y和W形成的三原子分子为![]() ,是直线形分子,该分子中心重合,为非极性分子,
,是直线形分子,该分子中心重合,为非极性分子,
故答案为:![]() ;非极性;
;非极性;
(2)![]() 分子中N原子价层电子对个数是4且含有一个孤电子对,所以该分子中中心原子杂化轨道类型为
分子中N原子价层电子对个数是4且含有一个孤电子对,所以该分子中中心原子杂化轨道类型为![]() 杂化,
杂化,![]() 的立体构型是三角锥形,故答案为:
的立体构型是三角锥形,故答案为:![]() ;三角锥形;
;三角锥形;
(3)![]() 是Mg元素,同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,Mg位于第三周期,该周期中第一电离能最大的主族元素是氯元素;熔沸点离子晶体
是Mg元素,同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,Mg位于第三周期,该周期中第一电离能最大的主族元素是氯元素;熔沸点离子晶体![]() 分子晶体,
分子晶体,![]() 是分子晶体、MgO是离子晶体,所以熔沸点
是分子晶体、MgO是离子晶体,所以熔沸点![]() ,
,
故答案为:氯元素;![]() ;
;
(4)该晶胞中阳离子个数![]() 、阴离子个数
、阴离子个数![]() ,所以阴阳离子个数之比
,所以阴阳离子个数之比![]() :
:![]() :1,
:1,
故答案为:2:1;
(5)![]() 晶胞为面心立方最密堆积,每个Cu原子周围距离最近的Cu原子数目
晶胞为面心立方最密堆积,每个Cu原子周围距离最近的Cu原子数目![]() ,
,
故答案为:12。

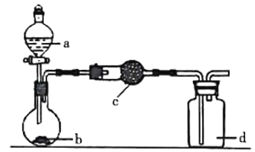
【题目】实验室中某些气体的制取、干燥及收集装置如图所示(省略夹持装置和尾气处理装置),仅用此装置和表中提供的物质完成相关实验,合理的是( )
选项 | a中物质 | b中物质 | c中干燥剂 | d收集气体 |
|
A | 浓硫酸 | 亚硫酸钠 | 无水氯化钙 | SO2 | |
B | 稀硫酸 | 大理石 | 无水氯化钙 | CO2 | |
C | 稀硝酸 | 铜片 | 碱石灰 | NO | |
D | 浓氨水 | 熟石灰 | 碱石灰 | NH3 |
A.AB.BC.CD.D