题目内容
 已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化:
已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
MnO2+C2O42-+4H+=Mn2++2CO2↑+2H2O
某研究小组为测定某软锰矿中MnO2的质量分数,准确称取1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液转移到容量瓶中并定容;从中取出25.00mL待测液置于锥形瓶中,再用0.0200mol?L-1KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应.试回答下列问题:
(1)0.0200mol?L-1KMnO4标准溶液应置于
甲
甲
(选填“甲”或“乙”)滴定管中;滴定终点如何判断当看到滴入一滴KMnO4溶液,锥形瓶中溶液立即变成紫色,且半分钟不褪色,即达到滴定终点
当看到滴入一滴KMnO4溶液,锥形瓶中溶液立即变成紫色,且半分钟不褪色,即达到滴定终点
.(2)你能否帮助该研究小组求得软锰矿中MnO2的质量分数
否
否
(选填“能”或“否”).若回答“能”,请给出计算结果否
否
;若回答“否”,试说明原因不知道容量瓶的规格
不知道容量瓶的规格
.(3)若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是
BC
BC
.A.溶液转移至容量瓶中,未将烧杯、玻棒洗涤
B.滴定前尖嘴部分有一气泡,滴定终点时消失
C.定容时,俯视刻度线
D.滴定前仰视读数,滴定后俯视读数
E.锥形瓶水洗之后未用待测液润洗.
分析:(1)KMnO4溶液呈紫色,草酸反应完毕,滴入最后一滴KMnO4溶液,紫色不褪去,滴定到终点,因高锰酸钾具有强氧化性,应装在酸式滴定管中;
(2)题中没有告诉使用的容量瓶的规格,无法知道配制的溶液的体积;
(3)A、没有洗涤烧杯、玻璃棒,导致配制的样品溶液的溶质物质的量减小;
B、滴定前有气泡,导致消耗的标准液体积增大;
C、定容时俯视刻度线,会导致配制的样品溶液的体积偏小,溶液的浓度偏大;
D、滴定前仰视读数,读数会偏大,滴定后俯视读数,读数会偏小,最终计算结果偏小;
E、锥形瓶不需要润洗,操作正确.
(2)题中没有告诉使用的容量瓶的规格,无法知道配制的溶液的体积;
(3)A、没有洗涤烧杯、玻璃棒,导致配制的样品溶液的溶质物质的量减小;
B、滴定前有气泡,导致消耗的标准液体积增大;
C、定容时俯视刻度线,会导致配制的样品溶液的体积偏小,溶液的浓度偏大;
D、滴定前仰视读数,读数会偏大,滴定后俯视读数,读数会偏小,最终计算结果偏小;
E、锥形瓶不需要润洗,操作正确.
解答:解:(1)高锰酸钾具有强氧化性,应装在酸式滴定管中,甲是酸式滴定管,乙是碱式滴定管;
草酸与酸性高锰酸钾发生氧化还原反应,当滴定到终点时,二者恰好完全反应,再滴入一滴KMnO4溶液变成紫色(或红色)且半分钟不褪色,可说明达到滴定终点,
故答案为:甲;当看到滴入一滴KMnO4溶液,锥形瓶中溶液立即变成紫色,且半分钟不褪色,即达到滴定终点;
(2)由于操作过程中没有告诉容量瓶的规格是多少,无法知道配制的溶液的体积,
故答案为:否;因为不知道容量瓶的规格;
(3)根据反应原理,消耗的高锰酸钾标准液体积偏大,高锰酸钾消耗的草酸根离子偏大,二氧化锰消耗的草酸根离子会偏小,测定的二氧化锰的含量偏小,
A.溶液转移至容量瓶中,未将烧杯、玻棒洗涤,没有洗涤烧杯、玻璃棒,会导致配制的样品溶液的溶质物质的量减小,滴定是消耗的高锰酸钾溶液偏小,测定的二氧化锰的含量结果偏高,故A错误;
B.滴定前尖嘴部分有一气泡,滴定终点时消失,滴定前有气泡,滴定时消耗的高锰酸钾标准液体积偏大,测定的二氧化锰含量偏低,故B正确;
C.定容时,俯视刻度线,会导致配制的样品溶液的体积偏小,溶液的浓度偏大,用高锰酸钾溶液滴定时,消耗的高锰酸钾溶液的体积偏大,测定的二氧化锰含量偏低,故C正确;
D.滴定前仰视读数,滴定后俯视读数:滴定前仰视读数,读数会偏大,滴定后俯视读数,读数会偏小,最终计算结果偏小,消耗的高锰酸钾溶液偏小,测定的二氧化锰含量偏高,故D错误;
E.锥形瓶水洗之后未用待测液润洗,锥形瓶不需要润洗,此操作正确,对滴定结果没有影响,故E错误;
故选BC.
草酸与酸性高锰酸钾发生氧化还原反应,当滴定到终点时,二者恰好完全反应,再滴入一滴KMnO4溶液变成紫色(或红色)且半分钟不褪色,可说明达到滴定终点,
故答案为:甲;当看到滴入一滴KMnO4溶液,锥形瓶中溶液立即变成紫色,且半分钟不褪色,即达到滴定终点;
(2)由于操作过程中没有告诉容量瓶的规格是多少,无法知道配制的溶液的体积,
故答案为:否;因为不知道容量瓶的规格;
(3)根据反应原理,消耗的高锰酸钾标准液体积偏大,高锰酸钾消耗的草酸根离子偏大,二氧化锰消耗的草酸根离子会偏小,测定的二氧化锰的含量偏小,
A.溶液转移至容量瓶中,未将烧杯、玻棒洗涤,没有洗涤烧杯、玻璃棒,会导致配制的样品溶液的溶质物质的量减小,滴定是消耗的高锰酸钾溶液偏小,测定的二氧化锰的含量结果偏高,故A错误;
B.滴定前尖嘴部分有一气泡,滴定终点时消失,滴定前有气泡,滴定时消耗的高锰酸钾标准液体积偏大,测定的二氧化锰含量偏低,故B正确;
C.定容时,俯视刻度线,会导致配制的样品溶液的体积偏小,溶液的浓度偏大,用高锰酸钾溶液滴定时,消耗的高锰酸钾溶液的体积偏大,测定的二氧化锰含量偏低,故C正确;
D.滴定前仰视读数,滴定后俯视读数:滴定前仰视读数,读数会偏大,滴定后俯视读数,读数会偏小,最终计算结果偏小,消耗的高锰酸钾溶液偏小,测定的二氧化锰含量偏高,故D错误;
E.锥形瓶水洗之后未用待测液润洗,锥形瓶不需要润洗,此操作正确,对滴定结果没有影响,故E错误;
故选BC.
点评:该题涉及到氧化还原滴定,虽然基于反应原理与中和滴定不同,但实验原理及操作和所用仪器等类似.由于该反应有明显的颜色变化,故可不可用指示剂.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
活性氧化锌常用作橡胶制品的硫化活性剂.工业上用粗氧化锌(含少量CuO、FeO、MnO、Fe2O3等)生产活性氧化锌,生产工艺流程如下:
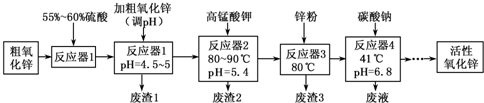
根据上表提供的信息,回答下列问题:
(1)“废渣1”的主要成分是 .
(2)完成“反应器2”中反应之一的离子方程式: MnO 4-+ Mn2++ = MnO2↓+ H+
(3)蘸取“反应器2”中的溶液点在 试纸上,如果观察到试纸变蓝,说明KMnO4过量.
(4)“废渣2”分离出的MnO2可用于制取MnO,已知:
2MnO2(s)+C(s)=2MnO(s)+CO2(g)△H=-174.6kJ?mol-1
C(s)+CO2(g)=2CO(g)△H=+283.0kJ?mol-1
试写出MnO2(s)与CO(g)反应制取MnO(s)的热化学方程式: .
(5)“反应器3”中加入锌粉的作用是 .
(6)“反应器4”得到的废液中,含有的主要离子除了Na+外,还有 .
(7)从“反应器4”中经过滤等操作得到碱式碳酸锌.取碱式碳酸锌3.41g,在400~450℃下加热至恒重,得到ZnO 2.43g和标准状况下CO2 0.224L,碱式碳酸锌的化学式为 .

| Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Mn(OH)2 | |
| 开始沉淀的pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
| 沉淀完全的pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
(1)“废渣1”的主要成分是
(2)完成“反应器2”中反应之一的离子方程式:
(3)蘸取“反应器2”中的溶液点在
(4)“废渣2”分离出的MnO2可用于制取MnO,已知:
2MnO2(s)+C(s)=2MnO(s)+CO2(g)△H=-174.6kJ?mol-1
C(s)+CO2(g)=2CO(g)△H=+283.0kJ?mol-1
试写出MnO2(s)与CO(g)反应制取MnO(s)的热化学方程式:
(5)“反应器3”中加入锌粉的作用是
(6)“反应器4”得到的废液中,含有的主要离子除了Na+外,还有
(7)从“反应器4”中经过滤等操作得到碱式碳酸锌.取碱式碳酸锌3.41g,在400~450℃下加热至恒重,得到ZnO 2.43g和标准状况下CO2 0.224L,碱式碳酸锌的化学式为