题目内容
【题目】关于氯气与过氧化钠在加热条件下的反应,在网上有三种不同的观点:
①氯气和过氧化钠均为强氧化剂,两者不反应。
②能反应,氯气是氧化剂。
③能反应,过氧化钠是氧化剂。为鉴别上述观点的真伪,进行了如下探究实验:

回答下列问题:
(1)过氧化钠的电子式为________,甲装置中发生反应的离子反应方程式为___。
(2)仪器戊的名称为___,其作用为___。
(3)为完成上述实验目的,仪器口连接顺序为a__。如果缺少丙装置, 乙装置中发生的反应为____。
(4)实验结束后,为验证观点②是否正确,需进一步进行的实验操作为___。
【答案】![]() 2MnO4-+16H++10Cl-=2Mn2++5 Cl2↑+8H2O 球形干燥管 防止空气中的水和二氧化碳进入装置乙,同时吸收多余的氯气 a→f→g→d→e→b→c(或c→b) →h 2Na2O2+2H2O===4NaOH+O2↑ 取装置乙中固体溶于稀硝酸中,加入硝酸银观察是否有白色沉淀产生或将带火星的木条置于i处,观察木条是否复燃。
2MnO4-+16H++10Cl-=2Mn2++5 Cl2↑+8H2O 球形干燥管 防止空气中的水和二氧化碳进入装置乙,同时吸收多余的氯气 a→f→g→d→e→b→c(或c→b) →h 2Na2O2+2H2O===4NaOH+O2↑ 取装置乙中固体溶于稀硝酸中,加入硝酸银观察是否有白色沉淀产生或将带火星的木条置于i处,观察木条是否复燃。
【解析】
(1)过氧化钠的电子式为![]() ,甲装置中发生化学方程式:
,甲装置中发生化学方程式:
2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8H2O,离子方程式:2MnO4-+16H++10Cl-=2Mn2++5 Cl2↑+8H2O。
(2)仪器戊的名称为球形干燥管,其作用为防止空气中的水和二氧化碳进入装置乙,同时吸收多余的氯气。
(3)为完成上述实验目的,在乙装置进行反应前需要将甲装置产生的气体净化除杂,仪器口连接顺序为a→f→g→d→e→b→c(或c→b) →h。如果缺少丙装置,甲装置中的水蒸气会进入乙装置中发生的反应为2Na2O2+2H2O===4NaOH+O2↑。
(4)实验结束后,为验证观点②是否正确,也就是证明氯气被还原为氯离子,过氧化钠被氧化为氧气,需进一步进行的实验操作为取装置乙中固体溶于稀硝酸中,加入硝酸银观察是否有白色沉淀产生或将带火星的木条置于i处,观察木条是否复燃。

【题目】二甲醚(CH3OCH3)是一种新型能源。
已知:①CO(g)+2H2(g)![]() CH3OH(g) △H1=﹣99kJ·mol-1
CH3OH(g) △H1=﹣99kJ·mol-1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=﹣24kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=﹣24kJ·mol-1
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H3=﹣41kJ·mol-1
CO2(g)+H2(g) △H3=﹣41kJ·mol-1
回答下列问题:
(1)写出CO和H2反应生成CO2和CH3OCH3(g)的热化学方程式_____。
(2)下列既能提高反应①中 CO 的平衡转化率,又能增大反应速率的是____(填标号)。
a.增大压强 b.降低温度 c.增大H2浓度 d.加高效催化剂
(3)在某恒温恒容容器中发生反应③,能说明该反应达到平衡的是___(填标号)。
a.气体平均相对分子质量保持不变
b.△H3保持不变
c.![]() 保持不变
保持不变
d.气体密度保持不变
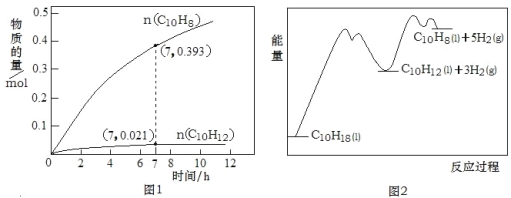
(4)在一定温度(T℃)下,向恒容密闭容器中通入一定量CH3OH气体,只发生反应②。气体混合物中CH3OCH3 的物质的量分数[φ(CH3OCH3)]与反应时间(t)有关数据如表所示。
t/min | 0 | 15 | 30 | 45 | 80 | 100 |
φ(CH3OCH3) | 0 | 0.05 | 0.08 | 0.09 | 0.10 | 0.10 |
①该温度下,上述反应的平衡常数K为___(用分数表示)。
②反应速率v=v正﹣v逆,其中v正=k正·φ2(CH3OH)、v逆=k逆·φ(CH3OCH3)·φ(H2O),k正、k 逆分别为正、逆反应速率常数,![]() 只与温度有关。15min时,=___(结果保留2位小数)。
只与温度有关。15min时,=___(结果保留2位小数)。
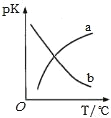
(5)在密闭容器中发生反应③,平衡常数为K。pK(pK=﹣lgK)与温度的关系如图所示,图中曲线___(填“a”或“b”)能反映平衡常数变化趋势。
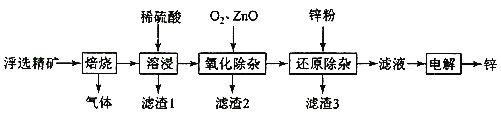
【题目】我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
请回答下列问题:
(1)焙烧过程中产生的气体化学式__。
(2)溶浸时,提高浸出率的方法有____。(至少写出两种)
(3)利用Fe(OH)3悬浊液与含SO2的烟气反应生成FeSO4,可以使烟气脱硫,该反应的离子方程式为__。产物FeSO4在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为__。
(4)氧化除杂时,加入ZnO调节溶液pH,当用广泛pH试纸测得pH值为___时,可认为已达除杂目的。
A.2 B.2.8 C.4 D.6.2
(5)滤渣3成分为______。
(6)若将闪锌矿直接浸入稀硫酸,要使0.10 molZnS完全溶于1LH2SO4(发生反应ZnS+H2SO4 =ZnSO4+H2S),则需H2SO4的最低浓度为___。(Ksp[ZnS]=2.5×10-22,H2S的K1=1×10-7,K2=1×10-14,忽略反应前后液体体积变化)