题目内容
7.电解CuSO4溶液时,要求达到三点:(1)阳极质量减少;(2)阴极质量增加;(3)电解质溶液中c(Cu2+)不变,则可选用的电极是( )| A. | 纯铜作阳极,含Zn和Ag的铜合金作阴极 | |
| B. | 含Zn和Ag的铜合金作阳极,纯铜作阴极 | |
| C. | 用纯铁作阳极,纯铜作阴极 | |
| D. | 用石墨作阴极,纯铜作阳极 |
分析 电解CuSO4溶液时,要求达到三点(1)阳极质量减少;(2)阴极质量增加;(3)电解质溶液中c(Cu2+)不变,则该装置是电镀池,铜作阳极、其它金属作阴极,电解质溶液为硫酸铜溶液,据此分析解答.
解答 解:电解CuSO4溶液时,要求达到三点(1)阳极质量减少;(2)阴极质量增加;(3)电解质溶液中c(Cu2+)不变,则该装置是电镀池,铜作阳极、其它金属作阴极,
A.纯铜作阳极、含Zn和Ag的铜合金作阴极,符合题目要求,故A正确;
B.根据A知,要实现题干要求,纯铜作阳极、含Zn和Ag的铜合金作阴极,故B错误;
C.纯铜作阴极、纯铁作阳极时,阳极质量减少、阴极质量增加,但溶液中铜离子浓度减小,所以不符合题目,故C错误;
D.用石墨作阴极,纯铜作阳极,符合题目要求,故D正确;
故选AD.
点评 本题以电解原理为载体考查电镀,明确电镀时阴阳极材料、电解质溶液特点即可解答,注意:活泼金属作阳极时,阳极上金属失电子发生氧化反应而不是溶液中阴离子失电子发生氧化反应,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列关于同系物的说法中,错误的是( )
| A. | 同系物具有相同的最简式 | |
| B. | 同系物之间相对分子质量相差14或14的整数倍 | |
| C. | 同系物符合同一通式 | |
| D. | 同系物的化学性质基本相似,物理性质随碳原子数的增加呈规律性变化 |
15.下列有关有机物的说法正确的是( )
| A. | (CH3CH2)2CHCH3的系统命名是2-乙基丁烷 | |
| B. | 葡萄糖在不同的条件下可以发生取代、加成、消去、氧化、还原、酯化反应 | |
| C. | 有机同系物具有相同的通式,且组成相差n个CH2,因此等质量的同系物完全燃烧耗氧相差物质的量为1.5nmol | |
| D. | 分离乙酸乙酯、乙酸、乙醇的混和物流程如下: |
2.对下列事实的解释正确的是( )
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性 | |
| B. | 向某溶液中加入氯化钡溶液和稀硝酸,生成白色沉淀,则原溶液一定含有SO42- | |
| C. | 常温下,将铜放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中钝化 | |
| D. | 浓硝酸在光照下变黄,证明硝酸不稳定,且产物有红棕色气体可溶于浓硝酸 |
19.下列离子方程式正确的是( )
| A. | 向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3•H2O+H2O | |
| B. | H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2 | |
| C. | 0.1mol/L CuCl2溶液中加入0.1mol/L NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S↑ | |
| D. | 用石墨作电极电解AlCl3溶液:2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$ Cl2↑+H2↑+2OH- |
16.下列涉及有机物的性质或应用的说法不正确的是( )
| A. | 干馏煤可以得到甲烷、苯和氨等重要化工原料 | |
| B. | 用于奥运“祥云”火炬的丙烷是一种清洁燃料 | |
| C. | 葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 | |
| D. | 蛋白质和油脂都是能发生水解反应的高分子化合物 |
17.下列关于元素周期表的说法正确的是( )
| A. | 每一周期的元素都从碱金属开始,最后以稀有气体结束 | |
| B. | 第二、三周期上下相邻的元素的原子核外电子数相差8个 | |
| C. | 只有第2列元素的原子最外层有2个电子 | |
| D. | 元素周期表共有十六个纵行,也就是十六个族 |
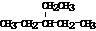 .
. 如图,曲线表示在800°C时,和某反应有关的物质A、B、C的物质的量浓度从开始反应至4分钟时的变化图象,试回答:
如图,曲线表示在800°C时,和某反应有关的物质A、B、C的物质的量浓度从开始反应至4分钟时的变化图象,试回答: