题目内容
12. 如图,曲线表示在800°C时,和某反应有关的物质A、B、C的物质的量浓度从开始反应至4分钟时的变化图象,试回答:
如图,曲线表示在800°C时,和某反应有关的物质A、B、C的物质的量浓度从开始反应至4分钟时的变化图象,试回答:(1)该反应的反应物是A.
(2)4分钟时,C的浓度是B的3倍.
(3)该反应的化学方程式是2A$\frac{\underline{\;800℃\;}}{\;}$B+3C
(4)反应开始至4分钟,若用A的浓度来表示该反应的平均速率为0.2mol/(L•min);用B的浓度来表示该反应的平均速率为0.1mol/(L•min).
(5)反应开始至4分钟,A的转化率为40%.
分析 (1)随反应进行,反应物的浓度降低,生成物的浓度增大,据此结合图象判断;
(2)根据图象可知4分钟时,C的浓度是1.2mol/L,B的浓度是0.4mol/L,据此答题;
(3)根据浓度变化量之比等于化学计量数之比确定化学计量数,t是达到平衡状态,为可逆反应,据此书写方程式;
(4)由图可知△c(A)=2.0mol/L-1.2mol/L=0.8mol/L,根据v=$\frac{△c}{△t}$计算A物质的平均反应速率,速率之比等于化学方程式计量数之比计算B的反应速率;
(5)转化率=$\frac{消耗量}{起始量}$×100%;
解答 解:(1)由图可知,随反应进行A的浓度降低,A为反应物,B、C的浓度增大,故B、C为生成物,故答案为:A;
(2)根据图象可知4分钟时,C的浓度是1.2mol/L,B的浓度是0.4mol/L,所以C的浓度是B的浓度的3倍,故答案为:3;
(3)由图可知,△c(A)=)=2.0mol/L-1.2mol/L=0.8mol/L,△c(B)=0.4mol/L,△c(C)=1.2mol/L,A、B、C化学计量数之比等于浓度变化量之比为0.8mol/L:0.4mol/L:1.2mol/L=2:1:3,反应为可逆反应,故反应方程式为2A$\frac{\underline{\;800℃\;}}{\;}$B+3C,
故答案为:2A$\frac{\underline{\;800℃\;}}{\;}$B+3C;
(4)由图可知△c(A)=2.0mol/L-1.2mol/L=0.8mol/L,所v(A)=$\frac{0.8mol/L}{4min}$=0.2mol/(L•min),V(B)=$\frac{1}{2}$V(A)=$\frac{1}{2}$×0.2mol/(L•min)=0.1mol/(L•min),
故答案为:0.2mol/(L•min);0.1mol/(L•min);
(5)A的转化率=$\frac{2.0mol/L-1.2mol/L}{2.0mol/L}$×100%=40%,故答案为:40%.
点评 本题考查化学反应速率、浓度-时间图象等,注重基础,旨在考查学生对基础知识的掌握,掌握基础和概念实质是关键,题目较简单.

| A. | CH3CH2CHBrCH3与氢氧化钠的乙醇溶液反应 | |
| B. | 甲苯在催化剂作用下与Cl2发生苯环上的取代反应 | |
| C. | 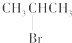 与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 | |
| D. | 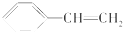 在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
| A. | 乙醚 | B. | 乙二醇 | C. | 丙三醇 | D. | 甲醇 |
| A. | 非金属元素之间形成的化合物一定是共价化合物 | |
| B. | 在气态单质分子中不一定存在着共价键 | |
| C. | 两个原子或多个原子之间的相互作用叫化学键 | |
| D. | 离子化合物中一定含有离子键,不存在共价键 |
| A. | 纯铜作阳极,含Zn和Ag的铜合金作阴极 | |
| B. | 含Zn和Ag的铜合金作阳极,纯铜作阴极 | |
| C. | 用纯铁作阳极,纯铜作阴极 | |
| D. | 用石墨作阴极,纯铜作阳极 |
| A. | 发展核能发电,以减少火力发电带来的SO2和CO2的排放问题 | |
| B. | 发展低碳经济,利用太阳能、风能实现城市照明 | |
| C. | 推行“限塑令”,研发用二氧化碳合成聚碳酸酯类可降解塑料 | |
| D. | 使用填埋法或焚烧法处理未经分类的生活垃圾 |
| A. | 2.8mol/L | B. | 3.0mol/L | C. | 3.2mol/L | D. | 3.6mol/L |

| A. | 步骤(2)产物中残留的烯丙醇可用溴水检验 | |
| B. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| C. | 苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| D. | 步骤(1)产物中残留的苯酚可用FeCl3溶液检验 |
