题目内容
14.由碳、氢、氧三种元素组成的某有机物分子中共含有13个原子,其原子核外共有40个电子,l mol该有机物在氧气中完全燃烧时需消耗5.5mol O2.请回答:(1)试求出该有机物的分子式.
(2)若该有机物可使溴水褪色,且分子中不含有甲基,也不能发生银镜反应,取0.1mol该有机物与足量钠反应,能产生1.12L H2(标准状况),则该有机物的结构简式可能是CH2=CHCH2CH2OH;该有机物在一定条件下发生聚合反应的化学方程式是
 .
.(3)若该有机物能发生银镜反应,且分子中只含有一个甲基,则其结构简式是CH3CH2CH2CHO.
(4)若该有机物的结构呈环状,且既不含甲基又不含羟基,则其键线式是
 .
.
分析 (1)设有机物的分子式为CxHyOz,1mol该有机物消耗氧气的物质的量为:(x+$\frac{y}{4}$-$\frac{z}{2}$)mol,分别根据原子数、核外电子总数及耗氧量列式计算;
(2)根据该有机物的分子式及限制条件写出满足条件的结构简式;
(3)能够发生有机反应,说明分子中含有醛基,再结合含有1个甲基确定其结构简式;
(4)若该有机物的结构呈环状,且既不含甲基又不含羟基,则该有机物没有侧链,据此写出其结构简式.
解答 (1)设有机物的分子式为CxHyOz,1mol该有机物消耗氧气的物质的量为:(x+$\frac{y}{4}$-$\frac{z}{2}$)mol=5.5,根据含有原子数可得:x+y+z=13,根据核外电子总数可得:6x+y+8z=40,联立解得:x=4、y=8、z=1,所以该有机物分子式为:C4H8O,
答:该有机物分子式为C4H8O;
(2)若该有机物可使溴水褪色,且分子中不含有甲基,也不能发生银镜反应,说明其分子中一定含有碳碳双键;
取0.1mol该有机物与足量钠反应,能产生1.12L H2(标准状况),氢气的物质的量为:$\frac{1.12L}{22.4L/mol}$=0.05mol,则该有机物分子中含有羟基的数目为:$\frac{0.05mol×2}{0.1mol}$=1,该有机物的结构简式为:CH2=CHCH2CH2OH;
该有机物分子中含有碳碳双键,能够发生加聚反应,反应的化学方程式为: ,
,
故答案为:CH2=CHCH2CH2OH; ;
;
(3)若该有机物能发生银镜反应,分子中含有醛基,且分子中只含有一个甲基,则其结构简式为:CH3CH2CH2CHO,
故答案为:CH3CH2CH2CHO;
(4)若该有机物的结构呈环状,且既不含甲基又不含羟基,则其分子中不含侧链,其结构简式为: ,
,
故答案为: .
.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握同分异构体的概念及书写原则,试题培养了学生的分析能力及化学计算能力.

| A. | .①②③ | B. | ①②⑥ | C. | ①④⑤⑥ | D. | ①②③⑥ |
| A. | 2-甲基丙烷 | B. | 异戊烷 | C. | 2,2-二甲基丁烷 | D. | 2,2-二甲基丙烷 |
| A. | 所有烷烃分子中均含有碳碳单键 | |
| B. | 苯及其同系物、醇类和羧酸都能发生取代反应 | |
| C. | 大气臭氧层的破坏主要与氟氯烃的氟原子有关 | |
| D. | 氨基酸与酸、碱都能发生反应生成盐 |
| A. | 乙醇(乙酸) 生石灰 过滤 | |
| B. | 乙醇(乙醛) 通入水蒸汽 催化加热 | |
| C. | 乙酸(乙醛) 通入O2气 常温常压 | |
| D. | 乙酸乙酯(乙酸) 碳酸钠溶液 分液 |

| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①③ |
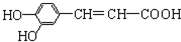 下列有关咖啡酸的说法中,不正确的是( )
下列有关咖啡酸的说法中,不正确的是( )| A. | 1mol咖啡酸可与3mol NaOH发生反应 | |
| B. | 咖啡酸可以发生还原、酯化、加聚、显色等反应 | |
| C. | 1mol咖啡酸可与4mol Br2发生反应 | |
| D. | 1mol咖啡酸最多可与5mol H2发生加成反应 |

 某产品只含C、H、O三种元素,分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).
某产品只含C、H、O三种元素,分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).