题目内容
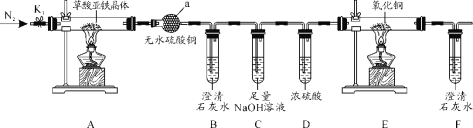
【题目】某校学生课外活动小组的同学设计如图所示实验装置,用来验证一氧化碳具有还原性,回答下列问题:(提示:C+CO2![]() 2CO C+H2O(g)
2CO C+H2O(g)![]() CO+H2)
CO+H2)

(1)写出装置A中所发生反应的离子方程式:____________。
(2)装置B中最适宜的试剂是________________。
(3)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是________。
(4)按照如图装置进行实验时,首先进行的操作是__________。
(5)根据实验中的___________现象,可证明CO具有还原性,有关反应的化学方程式是:__________。
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在图中装置_____与________之间连接图中的________装置(填序号)。
①![]() NaHCO3溶液 ②
NaHCO3溶液 ② 碱石灰 ③
碱石灰 ③![]() NaOH溶液 ④
NaOH溶液 ④![]() 浓H2SO4
浓H2SO4
【答案】CaCO3+2H+═Ca2++H2O+CO2↑ 饱和的碳酸氢钠溶液 没有除去气体中的水蒸气,高温下水蒸气与炭反应生成H2和CO,H2也能还原CuO,从而干扰对CO还原性的验证 检查装置气密性 E装置中黑色CuO变成红色 CO+CuO![]() Cu+CO2 D E ②
Cu+CO2 D E ②
【解析】
本题是探究CO还原性的实验设计题,利用C和CO2反应生成的CO还原氧化铜,结合氧化铜变红色粉末和石灰水变浑浊来推测CO的还原性,但因CO2中混有的水汽也能和C反应生成CO和H2,生成的H2有还原性对实验有干扰,因此CO2必须干燥处理。
(1)装置A中是盐酸和石灰石反应生成二氧化碳、氯化钙和水,其反应离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑;
(2)实验室用盐酸和石灰石制取二氧化碳,该反应放出的热量导致盐酸挥发,所以制取的二氧化碳中含有氯化氢气体,为除去氯化氢气体,选取的试剂应能除去氯化氢气体且不和二氧化碳反应,则只能选取可溶性的饱和碳酸氢盐,一般常用饱和的碳酸氢钠溶液;
(3)实验中没有装置C,使装置B与装置D直接相连,则CO2中混有的水汽会与碳反应生成还原性的H2,影响CO还原性的判断;
(4)因存在气体制备,整套实验装置需密封,故实验前,需对整套装置进行气密性检验;
(5)利用E装置中的黑色氧化铜变为红色,可知道氧化铜被还原为铜,推测CO具有还原性,发生反应的化学方程式为CO+CuO![]() Cu+CO2;
Cu+CO2;
(6)和二氧化碳的反应中,二氧化碳不可能完全转化为一氧化碳,所以从D装置出来的气体中含有二氧化碳,为防止原来二氧化碳的干扰,应先把D出来的二氧化碳除去,再将一氧化碳气体通过E装置,二氧化碳是酸性氧化物,所以用碱性物质除去,所以选②。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案【题目】无机化合物可根据其组成和性质进行分类
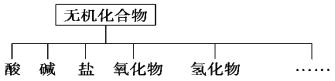
(1)图中所示的物质分类方法的名称是________。
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后面。
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ②____ | ③________ ④Ba(OH)2 | ⑤Na2CO3 ⑥______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(3)写出⑦转化为⑤的化学方程式:___________。
(4)实验室制备⑦常用______和______反应,检验该气体的方法是____________。
【题目】在20 L的密闭容器中按物质的量之比为1∶2充入CO和H2,发生反应:CO(g)+2H2(g)![]() CH3OH(g) ΔH。测得CO的转化率随温度及不同压强下的变化如图所示,p2和195 ℃时n(H2)随时间的变化结果如表所示。下列说法正确的是( )
CH3OH(g) ΔH。测得CO的转化率随温度及不同压强下的变化如图所示,p2和195 ℃时n(H2)随时间的变化结果如表所示。下列说法正确的是( )
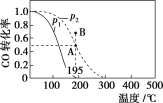
p2及195 ℃ 时n(H2)随时间变化
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 5 | 4 | 4 |
A. p1>p2,ΔH<0
B. 在p2及195 ℃ 时,反应前3 min的平均速率v(CH3OH)=0.8 mol·L-1·min-1
C. 在p2及195 ℃ 时,该反应的平衡常数为25
D. 在B 点时,v正>v逆