��Ŀ����
12������������������Ӧ�ù㷺��ʵ���ҿ���MnO2��Ũ���ᷴӦ��ȡ����Ӧԭ�����£�
MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O
��1�����Ƶñ�״����11.2L Cl2����������HClΪ1mol��
��2���������������NaOH��Һ���գ���Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O����ҵ��Ҳ����MnSO4��Һ�������������Mn2O3��Mn2O3�㷺Ӧ���ڵ��ӹ�ҵ��ӡȾ��ҵ��������д���û�ѧ��Ӧ�����ӷ���ʽ2Mn2++Cl2+3H2O�TMn2O3+6H++2Cl-��
��3�������̲��ŷḻ���̽�˿�����Ҫ�ɷ���MnO2��1991����Allen�����о�����������ϴ��ʹ�ò�ͬ�ķ������Ʊ�������MnO2�����Ʊ�������ͼ��ʾ��
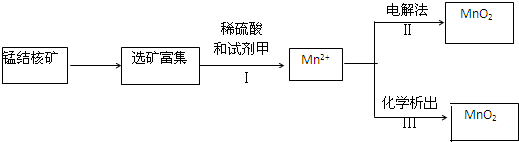
�ٲ���I�У��Լ��ױ�����е�������b������ţ���
a�������� b����ԭ�� c������
�ڲ�����У���NaClO3Ϊ��������������0.050mol MnO2ʱ������0.10mol•L-1 ��NaClO3��Һ200mL���÷�Ӧ�����ӷ���ʽΪ2ClO3-+5 Mn2++4H2O=5MnO2+Cl2��+8H+��
��4����100mL 12.0mol•L-1��Ũ����������MnO2��Ϻ��ȣ���Ӧ�������������ʵ���ԶԶ����0.30mol������������ܵ�ԭ��Ϊ���ŷ�Ӧ�Ľ��У�����Ũ�ȼ�С����Ӧ��ֹ��
���� ���⿼��������ʵ�����Ʊ�ԭ���ķ�������NaOH��Һ��MnSO4��Һ����β�������̽����MnO2�IJ�ͬ�Ʒ��������ǽ�+2����ѡ����������ͨ�����ķ������������õ����ص㿼���ͨ�����ӷ���ʽ���۷�Ӧԭ����
��1�������n��Cl2��=$\frac{11.2L}{22.4L/mol}$=0.5mol������Clԭ���غ���㱻����HCl�����ʵ�����
��2��Cl2��NaOH��Һ��Ӧ����NaCl��NaClO��ˮ�������ӱ�������������Mn2O3�����
��3�������������£�MnO2����ԭ���� Mn2+�������������ԭ�������л�ԭ�ԣ����������ӵ���Һ���õ�ⷨ����MnO2��Ҳ��������Һ�м���NaClO3�������ӱ���ԭ����MnO2��
�ڸ���ת�Ƶ����غ��ж�ClԪ�ز����ת�Ƶ����غ㡢Ԫ���غ㡢ԭ���غ���ƽ����ʽ��
��4������ϡ������������̲���Ӧ�����жϣ�
��� �⣺��1�������n��Cl2��=$\frac{11.2L}{22.4L/mol}$=0.5mol������Clԭ���غ���㱻����n��HCl��=2n��Cl2��=2��0.5mol=1mol���ʴ�Ϊ��1��
��2��Cl2��NaOH��Һ��Ӧ����NaCl��NaClO��ˮ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O�������ӱ�������������Mn2O3�����ᣬ���ӷ���ʽΪ2 Mn2++Cl2+3H2O�TMn2O3+6 H++2Cl-��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��2 Mn2++Cl2+3H2O�TMn2O3+6 H++2Cl-��
��3�����������£�MnO2����ԭ���� Mn2+�������������ԭ�������л�ԭ�ԣ����������ӵ���Һ���õ�ⷨ����MnO2��Ҳ��������Һ�м���NaClO3�������ӱ���ԭ����MnO2��
��ͨ�����Ϸ���֪�������ʾ��л�ԭ�ԣ���ѡb��
������0.050molMnO2ʱ������0.10mol•L-1��NaClO3��Һ200mL��n��NaClO3��=0.10mol/L��0.2L=0.02mol������Mnԭ���غ��n��Mn2+��=n��MnO2��=0.05mol��ת�Ƶ������ʵ���=0.05mol��2=0.1mol��Ҫת��0.1mol���ӣ���ClԪ�ػ��ϼ���+5�۱�Ϊ0�ۣ���������������n��Mn2+����n��NaClO3��=0.05mol��0.02mol=5��2���ٽ��ԭ���غ���ƽ����ʽΪ���ʴ�Ϊ��2ClO3-+5 Mn2++4H2O=5MnO2+Cl2��+8H+��
��4����100mL12.0mol•L-1��Ũ����������MnO2��Ϻ��ȣ����ŷ�Ӧ�Ľ��У������Ũ�����ͣ���ԭ�������������ɵ����������ʵ���С��0.30mol���ʴ�Ϊ�����ŷ�Ӧ�Ľ��У�����Ũ�ȼ�С����Ӧ��ֹ��
���� ���⿼�������Ʊ����������ʣ�Ϊ��Ƶ���㣬���ؿ���������ԭ��Ӧ�����ӷ���ʽ����д���ѵ��ǣ�3����ڲ�����жϣ�ע��ԭ���غ㡢ת�Ƶ����غ�����ã���Ŀ�ѶȲ���

| A�� | SO2��Cl2���ͨ��ˮ�к����ʹƷ����ɫ | |
| B�� | ����������ŷŻᵼ�¹⻯ѧ����������IJ��� | |
| C�� | ����������Ȼ��ֻ�Ի���̬���� | |
| D�� | Ũ�������������SO2��CO��Cl2������ |
| A�� | ���ʹ���������оƬ���ά | |
| B�� | 84����Һ����Ч�ɷ���NaClO | |
| C�� | SO2����Ư���ԣ�ͨ����ɫʯ����Һ����ʹ��Һ�ȱ�����ɫ | |
| D�� | ��ͨ��������ɿ���Na2O•CaO•6SiO2��ʾ���Ǵ����� |


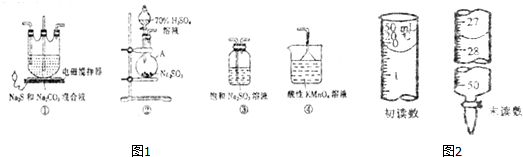

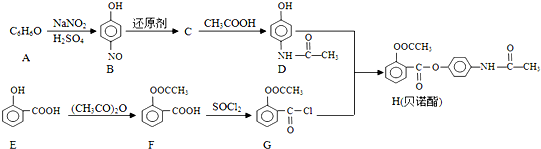
 ��
�� ��
�� ��
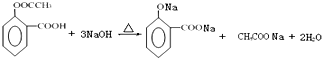
�� �ĺϳ�·������ͼ�����Լ�����ѡ����
�ĺϳ�·������ͼ�����Լ�����ѡ����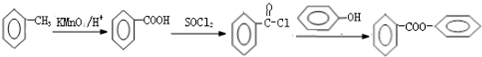 ��
��