题目内容
7.下列化学反应对应的离子方程式书写正确的是( )| A. | 漂白粉溶液在空气中生效:Ca2++2ClO-+CO2+H2O=2HClO+CaCO3↓ | |
| B. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH- | |
| C. | 氯化铁溶液与铜反应:Fe3++Cu=Fe2++Cu2+ | |
| D. | 0.01 mol•L-1NH4Al(SO4)2溶液与0.02 mol•L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O |
分析 A.次氯酸钙与二氧化碳、水反应生成次氯酸和碳酸钙;
B.酸性环境下不能生成氢氧根离子;
C.电荷不守恒;
D.NH4Al(SO4)2与Ba(OH)2安照物质的量之比1:2反应生成硫酸钡、一水合氨和氢氧化铝.
解答 解:A.漂白粉溶液在空气中失效离子方程式:Ca2++2ClO-+CO2+H2O=2HClO+CaCO3↓,故A正确;
B.用KIO3氧化酸性溶液中的KI,离子方程式:5I-+IO3-+6H+=3I2+3H2O,故B错误;
C.氯化铁溶液与铜反应:2Fe3++Cu=2Fe2++Cu2+,故C错误;
D.NH4Al(SO4)2与Ba(OH)2安照物质的量之比1:2反应生成硫酸钡、一水合氨和氢氧化铝,离子方程式:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O,故D正确;
故选:AD.
点评 本题考查了离子方程式的书写,明确反应实质、离子方程式书写方法是解题关键,注意反应物用量对反应的影响,选项D为易错选项.

练习册系列答案
相关题目
2. 铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
(一)高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
(1)该反应的平衡常数表达式K=$\frac{c(C{O}_{2})}{c(CO)}$;△H<0(填“>”、“<”或“=”).
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是B.
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正>υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=0.008 mol/(L•min).
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是KClO;生成0.5mol K2FeO4转移电子的物质的量是1.5mol.
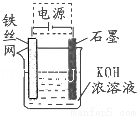
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示.电解过程中阳极的电极反应式为Fe+8OH--6e-═FeO42-+4H2O.
 铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:(一)高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是B.
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正>υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=0.008 mol/(L•min).
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是KClO;生成0.5mol K2FeO4转移电子的物质的量是1.5mol.
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示.电解过程中阳极的电极反应式为Fe+8OH--6e-═FeO42-+4H2O.
12.化学与社会、生产、生活密切相关,下列说法正确的是( )
| A. | 澳大利亚学者研究发现,夏季给鸡喂食碳酸水会使蛋壳变厚 | |
| B. | 陶瓷、水泥及所有玻璃都是硅酸盐产品 | |
| C. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| D. | Cl2有漂白性,所以用Cl2可与石灰乳反应制备含氯消毒剂 |
19.在一定温度下,可逆反应:A(g)+3B(g)?2C(g)达到化学平衡的标志是( )
| A. | C的生成速率与C的分解速率相等 | |
| B. | A、B、C的分子数之比是1:3:2 | |
| C. | 单位时间内生成n molA,同时生成3n mol B | |
| D. | A、B、C的浓度相等 |
16.下列化学用语正确的是( )
| A. | 乙酸根离子的结构式: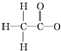 | |
| B. | CO2分子的球棍模型: | |
| C. | 3-甲基-1-丁烯的结构简式:(CH3)2CHCH=CH2 | |
| D. | 醛基的电子式为 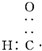 |
17.一定条件下反应A(s)+3B(g)?2C(g) 在10L的密闭容器中进行,测得2min内,A的物质的量由20mol减小到8mol,则下列说法中正确的是( )
| A. | 继续加入反应物A 2mol,反应速率一定加快 | |
| B. | 温度升高,反应速率一定加快 | |
| C. | 用反应物B表示该反应的反应速率为1.8 mol•L-1•min-1 | |
| D. | 用反应物C表示该反应的反应速率为3.6 mol•L-1•min-1 |

 .
.