��Ŀ����
��¯������ұ��������Ҫ��������������Ҫ��ӦΪ��
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ��H =" a" kJ mol��1
2Fe(s)+3CO2(g) ��H =" a" kJ mol��1
��1����֪��
��Fe2O3(s)+3C(ʯī) = 2Fe(s)+3CO(g) ��H1 =" +" 489.0 kJ mol��1
��C(ʯī)+CO2(g) = 2CO(g) ��H2 =" +" 172.5 kJ mol��1
��a = kJ mol��1��
��2��ұ������Ӧ��ƽ�ⳣ������ʽK = ���¶����ߺ�Kֵ ������������䡱��С������
��3����T��ʱ���÷�Ӧ��ƽ�ⳣ��K=64����2L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⡣
�� ��������CO��ƽ��ת����Ϊ ��
�� ����˵����ȷ���� ������ĸ����
a���������������ܶȺ㶨ʱ����־��Ӧ�ﵽƽ��״̬
b����������CO��ƽ��ת���ʴ����ҵ�
c���ס��������У�CO��ƽ��Ũ��֮��Ϊ2��3
d������Fe2O3�������CO��ת����
��4����ȡһ����ʩ�ɷ�ֹ������ʴ������װ���е��ձ����ʢ�е�Ũ�ȡ��������NaCl��Һ��
����a��cװ���У��ܱ��������� ������ĸ����
������dװ�ñ�������X���ĵ缫����Ӧ�� �������ƣ���
Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g) ��H =" a" kJ mol��1
2Fe(s)+3CO2(g) ��H =" a" kJ mol��1��1����֪��
��Fe2O3(s)+3C(ʯī) = 2Fe(s)+3CO(g) ��H1 =" +" 489.0 kJ mol��1
��C(ʯī)+CO2(g) = 2CO(g) ��H2 =" +" 172.5 kJ mol��1
��a = kJ mol��1��
��2��ұ������Ӧ��ƽ�ⳣ������ʽK = ���¶����ߺ�Kֵ ������������䡱��С������
��3����T��ʱ���÷�Ӧ��ƽ�ⳣ��K=64����2L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⡣
| | Fe2O3 | CO | Fe | CO2 |
| ��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ��/mol | 1.0 | 2.0 | 1.0 | 1.0 |
�� ��������CO��ƽ��ת����Ϊ ��
�� ����˵����ȷ���� ������ĸ����
a���������������ܶȺ㶨ʱ����־��Ӧ�ﵽƽ��״̬
b����������CO��ƽ��ת���ʴ����ҵ�
c���ס��������У�CO��ƽ��Ũ��֮��Ϊ2��3
d������Fe2O3�������CO��ת����
��4����ȡһ����ʩ�ɷ�ֹ������ʴ������װ���е��ձ����ʢ�е�Ũ�ȡ��������NaCl��Һ��
����a��cװ���У��ܱ��������� ������ĸ����
������dװ�ñ�������X���ĵ缫����Ӧ�� �������ƣ���

��1��-28.5 ��2��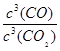 ��С
��С
��3����60% ��ac��©ѡ��1�֣���ѡ���÷֣�
��4����bc��©ѡ��1�֣���ѡ���÷֣� ��п
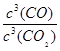 ��С
��С��3����60% ��ac��©ѡ��1�֣���ѡ���÷֣�
��4����bc��©ѡ��1�֣���ѡ���÷֣� ��п
�����������1�����ݸ�˹���ɿ�֪?H=��H1 -3��H2=-28.5kJ?mol?1������a="-28.5" ��
��2����ΪFe��Fe2O3Ϊ���壬����ƽ�ⳣ������ʽΪ��
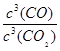 ����Ϊ�÷�ӦΪ���ȷ�Ӧ�������¶����ߣ�ƽ�������ƶ���Kֵ��С��
����Ϊ�÷�ӦΪ���ȷ�Ӧ�������¶����ߣ�ƽ�������ƶ���Kֵ��С����3���ٸ�������ʽ���м��㣺������һ����̼���ʵ���Ϊx
Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g��
��ʼ����mol�� 1 1
�仯����mol�� x x
ƽ������mol�� 1-x 1+x
K=
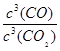 =
=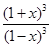 =64������õ�x=0.6����ת����=60%
=64������õ�x=0.6����ת����=60%��a����Ӧǰ�����������仯��������䣬�������������ܶȺ㶨ʱ����־��Ӧ�ﵽƽ��״̬����ȷ��b����������һ����̼���ӣ��൱������ѹǿ����Ӧǰ��������䣬��������CO��ƽ��ת���ʵ����ҵ�ת���ʴ���c����������ƽ��һ����̼���ʵ���Ϊ0.4mol���������н��ƽ�ⳣ������õ�����һ����̼Ϊ1.4mol��ƽ�����ʵ���Ϊ0.6mol������������CO��ƽ��Ũ��֮��Ϊ0.4+0.6=2��3����ȷ��d�����������Ӳ�Ӱ�컯ѧƽ�⣬����Fe2O3�������CO��ת���ʣ���d���ʴ�Ϊ��ac ��
��4����װ����ԭ��ص������͵��ص��������Եõ�������bc���Ա��������ʴ�Ϊ��bc��
��װ��Ϊԭ��أ�����dװ�ñ�������X���ĵ缫����Ӧ�������ÿ���ѡ��п��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ


 ��������Ӧ��Ӧ�Ļ�ѧ����ʽΪ ��
��������Ӧ��Ӧ�Ļ�ѧ����ʽΪ �� CH3OH(g) ��H1����90��7kJ��mol��1
CH3OH(g) ��H1����90��7kJ��mol��1
 CH3OH(g)
CH3OH(g)

 CH3OH(g) ��H= ��90��8kJ/mol
CH3OH(g) ��H= ��90��8kJ/mol _________
_________ ���>������<����=������
���>������<����=������