题目内容
氢氟酸(HF)是一种弱酸。25℃时,向20mL0.1mol/L氢氟酸中加入VmL 0.1mol/LNaOH溶液充分反应。已知:
HF(aq)+OH-(aq)=F-(aq)+H2O(l) △H=-67.7kJ/mol
H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol
根据题意,下列判断或结论正确的是
HF(aq)+OH-(aq)=F-(aq)+H2O(l) △H=-67.7kJ/mol
H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol
根据题意,下列判断或结论正确的是
| A.氢氟酸的电离过程是吸热的 |
| B.当V=20时,溶液中:c(F-)<c(Na+)=0.1mol/L |
| C.当V<20时,溶液中离子浓度关系可能为:c(Na+)=c(F-) |
| D.当V>20时,溶液中离子浓度关系一定为:c(Na+)>c(F-)>c(OH-)>c(H+) |
C
试题分析:A、已知①HF(aq)+OH-(aq)=F-(aq)+H2O(l) △H=-67.7kJ/mol。②H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol,则依据盖斯定律可知①-②即得到HF(aq)
 F-(aq)+H+(aq),所以△H=-67.7kJ/mol+57.3kJ/mol=-10.0kJ/mol,因此氢氟酸的电离过程是放热的,A不正确;B、当V=20时,二者恰好中和生成氟化钠,F-水解溶液显碱性,所以溶液中:c(F-)<c(Na+)=
F-(aq)+H+(aq),所以△H=-67.7kJ/mol+57.3kJ/mol=-10.0kJ/mol,因此氢氟酸的电离过程是放热的,A不正确;B、当V=20时,二者恰好中和生成氟化钠,F-水解溶液显碱性,所以溶液中:c(F-)<c(Na+)= ×0.1mol/L=0.05mol/L,B不正确;C、当V<20时,氢氟酸过量,因此所得溶液可能显中性。则根据电荷守恒可知c(Na+)+ c(H+)=c(F-)+c(OH-),所以溶液中离子浓度关系可能为:c(Na+)=c(F-),C正确;D、当V>20时,氢氧化钠过量,溶液显碱性,则溶液中离子浓度关系可能为:c(Na+)>c(OH-)>c(F-)>c(H+),D不正确,答案选C。
×0.1mol/L=0.05mol/L,B不正确;C、当V<20时,氢氟酸过量,因此所得溶液可能显中性。则根据电荷守恒可知c(Na+)+ c(H+)=c(F-)+c(OH-),所以溶液中离子浓度关系可能为:c(Na+)=c(F-),C正确;D、当V>20时,氢氧化钠过量,溶液显碱性,则溶液中离子浓度关系可能为:c(Na+)>c(OH-)>c(F-)>c(H+),D不正确,答案选C。
练习册系列答案
相关题目




 ①
①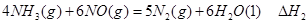 ②
② ③
③ 、
、 、
、 三者之间关系的表达式,
三者之间关系的表达式,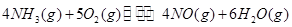
 =
=







 2 Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
2 Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol

 H= -221.0kJ/mmol
H= -221.0kJ/mmol 2Fe(s)+3CO2(g) ΔH =" a" kJ mol-1
2Fe(s)+3CO2(g) ΔH =" a" kJ mol-1
 O2(g)= ZnO (s) △H=" -" Q1 kJ? mol-1 ①
O2(g)= ZnO (s) △H=" -" Q1 kJ? mol-1 ①