题目内容
用石灰乳、石灰氮(CaCN2)和炼厂气(含H2S)反应,既能净化尾气,又能获得应用广泛的CS(NH2)2(硫脲),其部分工艺流程如下:
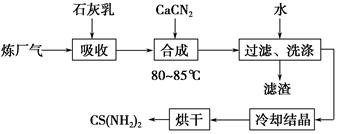
(1)高温下,H2S存在下列反应:2H2S(g)??2H2(g)+S2(g),其平衡常数表达式为K=________________。
(2)用石灰乳吸收H2S制取Ca(HS)2需要在低温下进行,其原因是_____________________________________________________;
过滤得到的滤渣可再利用,滤渣的主要成分是________(填化学式)。
(3)合成硫脲需长时间搅拌,并在较高温度(80~85 ℃)下进行,其目的是_______________________________________。
Ca(HS)2与CaCN2在水溶液中合成硫脲的化学方程式为________________________________。
(4)化合物X与硫脲互为同分异构体,X加入FeCl3溶液中,溶液显红色,X的化学式为________________。

(1)高温下,H2S存在下列反应:2H2S(g)??2H2(g)+S2(g),其平衡常数表达式为K=________________。
(2)用石灰乳吸收H2S制取Ca(HS)2需要在低温下进行,其原因是_____________________________________________________;
过滤得到的滤渣可再利用,滤渣的主要成分是________(填化学式)。
(3)合成硫脲需长时间搅拌,并在较高温度(80~85 ℃)下进行,其目的是_______________________________________。
Ca(HS)2与CaCN2在水溶液中合成硫脲的化学方程式为________________________________。
(4)化合物X与硫脲互为同分异构体,X加入FeCl3溶液中,溶液显红色,X的化学式为________________。
(1) 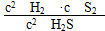 (2)温度低H2S溶解量大,溶液中H2S浓度高,有利于吸收 Ca(OH)2[或Ca(OH)2和CaS] (3)使反应物充分接触,维持较高温度,有利于提高反应速率 Ca(HS)2+2CaCN2+6H2O
(2)温度低H2S溶解量大,溶液中H2S浓度高,有利于吸收 Ca(OH)2[或Ca(OH)2和CaS] (3)使反应物充分接触,维持较高温度,有利于提高反应速率 Ca(HS)2+2CaCN2+6H2O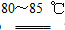 2CS(NH2)2+3Ca(OH)2 (4)NH4SCN
2CS(NH2)2+3Ca(OH)2 (4)NH4SCN
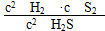 (2)温度低H2S溶解量大,溶液中H2S浓度高,有利于吸收 Ca(OH)2[或Ca(OH)2和CaS] (3)使反应物充分接触,维持较高温度,有利于提高反应速率 Ca(HS)2+2CaCN2+6H2O
(2)温度低H2S溶解量大,溶液中H2S浓度高,有利于吸收 Ca(OH)2[或Ca(OH)2和CaS] (3)使反应物充分接触,维持较高温度,有利于提高反应速率 Ca(HS)2+2CaCN2+6H2O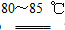 2CS(NH2)2+3Ca(OH)2 (4)NH4SCN
2CS(NH2)2+3Ca(OH)2 (4)NH4SCN (1)该反应的反应物和生成物均为气体,K的表达式为生成物浓度的次方除以反应物浓度的次方。(2)气体在水中的溶解度随着温度的升高而减小。石灰乳中Ca(OH)2的浓度较大,吸收H2S后,一般仍有剩余,可以再利用。(3)接触面积大,温度高均可以提高反应速率。由(2)的提示知,石灰乳吸收H2S生成Ca(HS)2进入“合成”阶段,箭头指入为加入反应物,则CaCN2和H2O均为反应物,由元素守恒知,生成CS(NH2)2外还有Ca(OH)2。(4)某溶液遇FeCl3溶液,溶液显红色,则该溶液中含有SCN-,互为同分异构体的两种化合物化学式相同,由原子种类和数目可以确定还有NH4+,则为NH4SCN。

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目



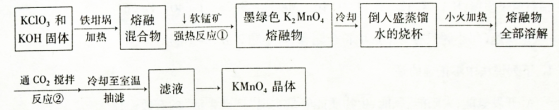



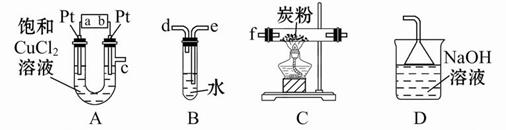
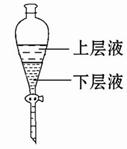
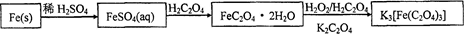
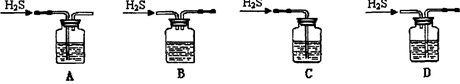
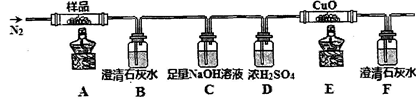
 溶液
溶液
 得固体b g
得固体b g
 量气测得气体体积Va mL
量气测得气体体积Va mL 250 mL溶液
250 mL溶液 三次平均消耗0.1 mol·L-1酸性KMnO4溶液Vb mL你认为以上方案中 无法确定样品的组成,理由是 。
三次平均消耗0.1 mol·L-1酸性KMnO4溶液Vb mL你认为以上方案中 无法确定样品的组成,理由是 。