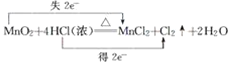
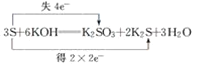
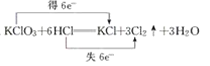
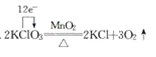
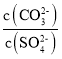��Ŀ����
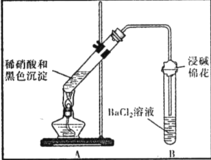
����Ŀ��ij��ȤС���ͭ��Ũ���ᷴӦ�����ĺ�ɫ���������ܺ���CuO��CuS��Cu2S������CuS�� Cu2S������ϡ���ᡢϡ���ᣩ����̽����ʵ�鲽�����£�
������ͭ˿����Ũ���ᣬ���ȣ�
������������ɫ����������ʱ�����ͭ˿��ֹͣ���ȣ�
����ȴ�ӷ�Ӧ��Ļ�����з������ɫ������ϴ�������ﱸ�á�
�ش��������⣺
��1��������������Ļ�ѧʽΪ______________��
��2������ Cu2+��Һ�еμ�K4[Fe(CN)6]��Һ���ܲ������ɫ�������ֽ�������ɫ��������ϡ�����У�������Ժ��ٵμ�K4[Fe(CN)6]��Һ��δ�����ɫ�������ɴ����ý�����______________��
��3��Ϊ֤����ɫ��������ͭ�������������ʵ�飺
װ�� | ���� | ���ۼ����� |
| ��A�Թ��к�ɫ�������ܽ� | a�������˵����ɫ��������_________�ԡ� |
��4��CuS�����������ȵ�Ũ���ᣬ�����й�ƽ���ƶ�ԭ�����Խ��ͣ�__________��
��5��Ϊ�ⶨ��ɫ������Cu2S �İٷֺ�����ȡ0.2g ��������ú�ɫ��������������Һ���� 40.0mL 0.075mol/L KMnO4��Һ������������Ӧ���£�
8MnO4��+5Cu2S+44H+�T10Cu2++5SO2��+8Mn2++22H2O
6MnO4��+5CuS+28H+�T5Cu2++5SO2��+6Mn2++14H2O
��Ӧ�������Һ���Ͼ�SO2�������ĸ��������Һǡ����35.0mL 0.1mol/L (NH4)2Fe(SO4)2��Һ��Ӧ��ȫ����������Cu2S ����������Ϊ____________________��
���𰸡�SO2 ��ɫ�����в�����CuO ��ԭ�� NO2+SO2+Ba2++H2O�TBaSO4��+NO��+2H+ CuS�����ܽ�ƽ��CuS��s��Cu2+��aq��+S2����aq�����ȵ�Ũ���ὫS2��������ʹS2��Ũ�ȼ�С���ٽ�����ƽ���������ƶ���ʹCuS�ܽ� 40%
��������
��1������ͭ��Ũ���ᷴӦ���ɶ�������������н��
��2������������Ϣ�м���ͭ���ӵķ����Ԣڽ��з�����Ȼ��ó���ȷ���ۣ�
��3��a������ɫ����Ϊ����������˵��ϡ���ᱻ��ԭ����һ����������ɫ������л�ԭ�ԣ�
b�����ݷ�Ӧ����ۿ�֪��ɫ������ϡ���ᷴӦ�����˶�������֤����ɫ�����к�����Ԫ�أ�������������������Ļ�������ܹ����Ȼ�����Ӧ�������ᱵ�������ݴ�д����Ӧ�����ӷ���ʽ��
��4��CuS����Һ�д��ڳ����ܽ�ƽ�⣬����ƽ���ƶ�������
��5�����ݵζ�ʵ�����ݼ���ʣ�����������ʵ������õ�������ͭ����ͭ��Ӧ�ĸ���������ʵ��������ݷ�Ӧ�����ӷ���ʽ��ʽ����õ���
��1��Cu��Ũ���ᷴӦ��������ͭ�����������ˮ����ӦΪCu+2H2SO4��Ũ��![]() CuSO4+2SO2��+2H2O������������������SO2���ʴ�ΪSO2��
CuSO4+2SO2��+2H2O������������������SO2���ʴ�ΪSO2��
��2������Һ�еμ�K4[Fe(CN)6]��Һ�����������ɫ������֤����Cu2+�����ݢڽ���ɫ��������ϡ�����У�һ��ʱ��μ� K4[Fe(CN)6]��Һ��δ�����ɫ������֪����ɫ������һ������CuO���ʴ�Ϊ��ɫ�����в�����CuO��
��3��a��A�Թ����Ϸ����ֺ���ɫ���壬˵����Ӧ����һ���������ɣ�֤���˺�ɫ������л�ԭ�ԣ��ڷ�Ӧ�б��������ʴ�Ϊ��ԭ�ԣ�
b�����ݷ�Ӧ�����B�Թ��г��ְ�ɫ������֪����ɫ����Ϊ���ᱵ��˵����ɫ�����к�����Ԫ�أ�������Ӧ�����ӷ���ʽΪ��NO2+SO2+Ba2++H2O�TBaSO4��+NO��+2H+���ʴ�ΪNO2+SO2+Ba2++H2O�TBaSO4��+NO��+2H+��
��4��CuS������ˮ����ˮ��Һ�л��к�������CuS�ܽ⣬��Һ�д��ڳ����ܽ�ƽ�⣬CuS��s��![]() Cu2+��aq��+S2����aq�����ȵ�Ũ���ὫS2��������ʹS2��Ũ�ȼ�С���ٽ�����ƽ���������ƶ���ʹCuS�ܽ⣻�ʴ�ΪCuS�����ܽ�ƽ��CuS��s��
Cu2+��aq��+S2����aq�����ȵ�Ũ���ὫS2��������ʹS2��Ũ�ȼ�С���ٽ�����ƽ���������ƶ���ʹCuS�ܽ⣻�ʴ�ΪCuS�����ܽ�ƽ��CuS��s��![]() Cu2+��aq��+S2����aq�����ȵ�Ũ���ὫS2��������ʹS2��Ũ�ȼ�С���ٽ�����ƽ���������ƶ���ʹCuS�ܽ⣻
Cu2+��aq��+S2����aq�����ȵ�Ũ���ὫS2��������ʹS2��Ũ�ȼ�С���ٽ�����ƽ���������ƶ���ʹCuS�ܽ⣻
��5�������ķ�ӦΪ��
8MnO4��+5Cu2S+44H+�T10Cu2++5SO2��+8Mn2++22H2O
6MnO4��+5CuS+28H+�T5Cu2++5SO2��+6Mn2++14H2O
MnO4��+5Fe2++8H+�TMn2++5Fe3++4H2O
��Cu2S��CuS�����ʵ����ֱ�Ϊx��y��
��Cu2S��CuS��Ӧ��ʣ��KMnO4�����ʵ�����0.035L��0.1mol/L��![]() =0.0007mol��
=0.0007mol��
160x+96y=0.2
![]() =0.04��0.075��0.0007
=0.04��0.075��0.0007
���x=0.0005mol��
Cu2S������������![]() ��100%=40%��
��100%=40%��

����Ŀ���ס��������ܱ������о�������Ӧ��C(s)��2H2O(g) ![]() CO2(g)��2H2(g)����H��0���й�ʵ���������±���ʾ��
CO2(g)��2H2(g)����H��0���й�ʵ���������±���ʾ��
���� | �ݻ�/L | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ƽ�ⳣ�� | |
C(s) | H2O(g) | H2(g) | |||||
�� | 2 | T1 | 2 | 4 | 3.2 | 3.5 | K1 |
�� | 1 | T2 | 1 | 2 | 1.2 | 3 | K2 |
����˵����ȷ����(����)
A.T1<T2B.�������У�����Ӧ���е�1.5 minʱ��n(H2O)��1.4 mol
C.���������ܶ�ʼ�ձ��ֲ���D.K2��1.35