��Ŀ����
����Ŀ����ѧʵ���벻��ˮ�������ˮ�IJ�ͬ���ú��ܣ����������ĸ�װ��ͼ���ش����⣺
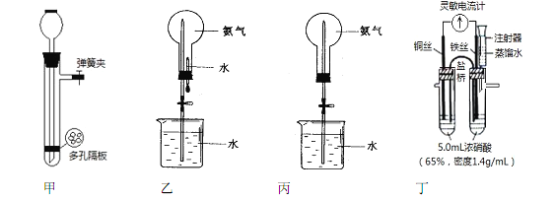
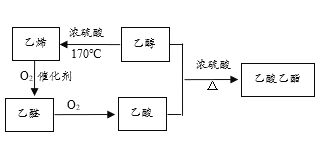
ʵ��һ����ȡ����
��1��ͼ����ʾװ�ÿ�����ʵ������ȡ��������������װ���ڼ��뷴Ӧ��ǰ����μ��������______��
��2����п��ϡ������ȡ����ʱ��������������ͭ��Һ��ӿ�������������ʣ�����ͼӿ췴Ӧ���ʵ�ԭ��________________________________��
ʵ�������Ȫʵ��
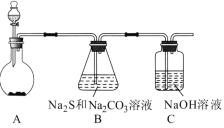
��3��ͼ����ʾװ������ƿ��װ�����ﰱ���� ������Ȫʵ��ʱӦ����___________����������ͷ�ι���������ֹˮ��������
��4�����ֻ�ṩ��ͼ����ʾװ�ã�����Ѹ��������Ȫ�����з������е���____________��
a������ë����ס��ƿ
b���ñ�����ס��ƿ
c�����ձ��е�ˮ���ɱ���ʳ��ˮ
d�����ձ��м�����������
ʵ������̽��һ���¶�����ʹ���ۻ�����������Ũ�ȣ�ʵ��װ����ͼ����ʾ��
����ʼʵ��ʱ���۲쵽����������ָ��ָ��ͭ˿������Ѹ�ٷ�תָ����˿��
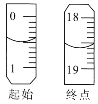
������ʢ����ˮ��ע�����������֧�Թ��ڼ�ˮ������ָ��ǡ�ÿ�ʼ��תָ��ͭ˿ʱֹͣʵ�飻
���ظ�����ʵ���ƽ����ˮ��Ϊ2.5 mL��ˮ���ܶȰ�1.0g/mL���㣩��
��5����ʵ��װ�õIJ���֮����__________________________________��
��6����ָ���һ��ָ��ͭ˿ʱ�������ĵ缫��ӦʽΪ_______________________________��
��7�����ݴ�ʵ����㣬ʹ���ۻ������������������Ϊ_______________________��
���𰸡�������Ƥ�����н����ɼк�������©���м�ˮ��ʹ©�����ܵ�Һ������Թܵ�Һ�棬Һ���ֲ���һ��ʱ�䣬˵������������ Zn��Cu2����Zn2����Cu���γ�пͭԭ��أ�ʹ��Ӧ���ʼӿ� ����ͷ�ι� ab û��β������װ�� NO3����e����2H����H2O��NO2�� 47.9%
��������
��1��װ�������Լ����ԭ���ǣ�ͨ�����巢�����븽���Һ�幹�ɷ����ϵ�����ݸı���ϵ��ѹǿʱ���������������ݵ����ɡ�ˮ�����γɡ�Һ��������ȣ����ж�װ�������Եĺû���
��2��ԭ����ܼӿ췴Ӧ���ʡ�
��3��Ȼ��ѹ��ͷ�ιܣ�ʹˮ������ƿ�У���������ˮ��ʹ��ƿ��ѹǿ���ͣ�Ȼ���ֹˮ�У�ˮ�ͻ����Ų����ܽ�����ƿ���γ���Ȫ��
��4��ֻҪʹ������ˮ�Ӵ��������γ���Ȫ��
��5��Ũ����Ļ�ԭ������NO2������Ⱦ������
��6����ָ���һ��ָ��ͭ˿ʱ�������������ۻ�������������õ�������NO2��
��7���������μ�ˮ����ƽ��ֵ��![]() ������ʹ���ۻ��������������������
������ʹ���ۻ��������������������
��1��װ����ʹ�õ��dz���©������������Ե�ʵ�������������Ƥ�����н����ɼк�������©���м�ˮ��ʹ©�����ܵ�Һ������Թܵ�Һ�棬Һ���ֲ���һ��ʱ�䣬˵�����������á�
��2������п�ܰ�����ͭ�е�ͭ�����û��������Ӷ�����пͭԭ��ض��ӿ췴Ӧ���ʣ���Ӧ�ķ���ʽΪZn��Cu2����Zn2����Cu��
��3������װ��ͼ���жϽ�����Ȫʵ��ʱӦ���ȼ���ͷ�ιܡ�
��4������ʱ��ƿ��ѹǿ��������������ͣ���������ˮ�Ӵ�ʱ��������������ˮ��������ƿ��ѹǿѸ�ټ�С���γ���Ȫ������ʹ��ƿ��ѹǿ���ͣ����������ѹ��ѹ�ˮ�������ƿ�кͰ����Ӵ�����ѡab��
��5������Ũ����Ļ�ԭ������NO2������ɴ�����Ⱦ����˸�ʵ��װ�õIJ���֮����û��β������װ�á�
��6����ָ���һ��ָ��ͭ˿ʱ��������������õ����ӣ��缫��ӦʽΪNO3����e����2H����H2O��NO2����
��7�����ݴ�ʵ����㣬ʹ���ۻ������������������Ϊ![]() 47.9%��
47.9%��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ�������й�˵����ȷ�ҽ��ͺ�������
˵�� | ���� | |
A | һ���¶�ѹǿ�£�2 g H2 �� 4 g H2 ��ȫȼ�գ����� ȼ���ȵ���ֵ�� | 4 g H2 �ų������� |
B | 2SO2(g)��O2(g) ƽ����ټ��� SO2��Q ���� | ƽ�����ƣ��ų��������� |
C | ������ʵ���Ũ�ȵ� NaI �� KBr ���Һ�еμ� AgNO3 ��Һ�������ɻ�ɫ AgI ���� | Ksp(AgI)��Ksp(AgBr) |
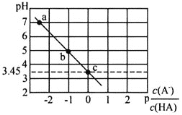
D | �����ʵ���Ũ�� Na2CO3 �� pH ���� CH3COONa | H2CO3 �����Ա� CH3COOH ǿ |
A.AB.BC.CD.D
����Ŀ����1��ʵ����5g�״�����������ȫȼ�գ����ɶ�����̼�����Һ̬ˮʱ�ͷų�113.5 kJ����������д���״�ȼ�յ��Ȼ�ѧ����ʽ��___________________________��
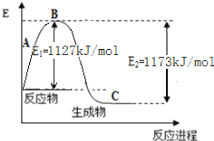
��2���ּ�֪N2(g)��H2(g)��Ӧ����1 molNH3(g)�����������仯ʾ����ͼ������������֪�������ݼ���N-H������Ϊ____________________kJ/mol ��
��ѧ�� | H-H |
|
����(kJ/mol) | 436 | 946 |
��3������ͼ��ʾװ�ý����к��Ȳⶨʵ�飬��ش��������⣺

����A������Ϊ ________________________ ��
ȡ30mLH2SO4��0.5mol��L-1����Һ��50mLNaOH��0.5mol��L-1����Һ��С�ձ��н����кͷ�Ӧ������ʵ���¶�ƽ������4.1������֪�кͺ����ɵ���Һ�ı�����Ϊ![]() ����Һ���ܶȾ�Ϊ1g/cm3��ͨ������ɵ��к��� ______ ��������С�����һλ��
����Һ���ܶȾ�Ϊ1g/cm3��ͨ������ɵ��к��� ______ ��������С�����һλ��
����ʵ����ֵ�����57.3kJ��mol-1��ƫ�������ƫ���ԭ������ǣ�����ĸ��______��
a��ʵ��װ�ñ��¡�����Ч����
b�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�
c��һ����NaOH��Һ����ʢ�������С�ձ���
ʵ����������60mLH2SO4��0.25mol��L-1����Һ��50mLNaOH��0.55 mol��L-1����Һ���з�Ӧ��������ʵ����ȣ����ų������� ______ �������������������������������к��� _____ ������������������������������50mL0.5mol��L-1�������H2SO4��Һ��������ʵ�飬��÷�Ӧǰ���¶ȵı仯ֵ�� ______ ������ƫ��������ƫС����������Ӱ��������