题目内容
【题目】在一定温度、压强下,向密闭容器中投入一定量N2和H2,发生反应:N2+3H2![]() 2NH3 △H<0。
2NH3 △H<0。
(1)反应开始阶段,v(正)_______(填“>”“<”或“=”)v(逆),随后v(正)________逐渐(填“增大”或“减小”,下同),v(逆)逐渐_______,反应达到平衡时,v(正)_______(填“>”“<”或“=”)v(逆)。
(2)达到平衡后,若正反应速率用v(N2)表示,逆反应速率用v’(H2)表示,则v(N2)=____v’(H2)。
(3)下列措施中能加快反应速率并提高氢气的转化率的是_______(填字母)。
A 其他条件不变时,压缩容器体积 B 其他条件不变时,升高反应体系温度
C 使用合适的催化剂 D 保持容器体积不变,充入一定量的氮气
(4)实际生产中往往需要将温度控制在一个合适的范围,分析温度不宜过高也不宜过低的原因是_____。
【答案】> 减小 增大 = ![]() AD 温度过低,化学反应速率慢,氨气的生成效率低;温度过高,平衡逆向移动,产物的转化率低。
AD 温度过低,化学反应速率慢,氨气的生成效率低;温度过高,平衡逆向移动,产物的转化率低。
【解析】
(1)反应开始时,加入N2和H2,反应朝着正反应方向进行, v(正)> v(逆);开始时,反应物浓度最大,随着反应的进行,反应物浓度减小,生成物浓度增大,则v(正)减小,v(逆)增大;达到平衡时,正反应速率等于逆反应速率,则v(正)= v(逆);
(2)达到平衡时,正反应速率等于逆反应速率,但是同一化学反应中,用不同的物质表示化学反应速率,其数值之比等于计量数之比,即v正(N2)=v逆(N2)=![]() v’(H2);
v’(H2);
(3) A、其他条件不变时,压缩容器体积,各反应物的浓度增大,化学反应速率增大;压缩体积,压强增大,平衡向气体体积减小的方向移动,即正反应方向移动,氢气转化率增大,A符合题意;
B、其他条件不变时,升高反应体系温度,升高温度,化学反应速率增大;升高温度,平衡向吸热反应方向移动,即逆反应方向移动,则H2的转化率减小,B不符合题意;
C、使用合适的催化剂,化学反应速率增大;但是催化剂不改变化学平衡,则H2的转化率不变,C不符合题意;
D、保持容器体积不变,充入一定量的氮气,反应物浓度增大,化学反应速率增加;增大反应物浓度,平衡正向移动,H2的转化率增加,D符合题意;
答案选AD;
(4)工业生产氨气,温度不能过低,温度过低,催化剂活性低,化学反应速率慢,氨气生产效率低下;合成氨反应是放热反应,温度过高,平衡逆向移动,反应物转化率低,所以温度需要控制在一定范围,不能过高也不能过低。

【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
已知化学键键能数据如表:
化学健 | C﹣H | C=O | H﹣H | C≡O(CO) | ||
键能(kJ/mol) | 413 | 745 | 436 | 1075 |
(1)①CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)。则该反应的△H=_____________。
2CO(g)+2H2(g)。则该反应的△H=_____________。
②在恒容绝热条件下,一定能说明该反应已达平衡状态的是_____________。(填字母)
A.混合气体的密度不再变化B.混合气体的平均相对分子质量不再变化
C.容器内的温度不再变化D.v正(CH4)=2v逆(H2)
(2)利用CO2可制取甲醇,其反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g);△H=-49.0KJ/mol;为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在恒温恒容密闭容器中,充入2molCO2和6molH2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图1所示。从反应开始到平衡,v(H2)=_____________;该温度下的平衡常数数值=_____________(保留三位有效数字)。
CH3OH(g)+H2O(g);△H=-49.0KJ/mol;为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在恒温恒容密闭容器中,充入2molCO2和6molH2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图1所示。从反应开始到平衡,v(H2)=_____________;该温度下的平衡常数数值=_____________(保留三位有效数字)。

(3)下列措施能使![]() 增大的是________。
增大的是________。
A.降低温度
B.恒温恒容下,再充入2molCO2、6molH2
C.使用高效催化剂
D.恒温恒容充入He(g)使体系压强增大
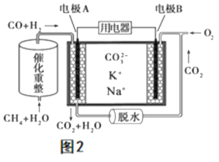
(4)一种熔融碳酸盐燃料电池原理示意如图2。
①该电池的负极反应式为_____________
②电池工作时,CO32﹣向电极_____________移动(填A或者B)。