题目内容
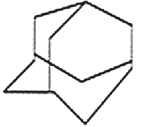
【题目】有机物的结构可用“键线式”简化表示。CH3—CH=CH-CH3可简写为 ![]() 。有机物X的键线式为:
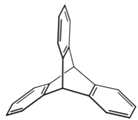
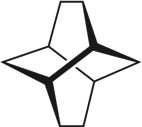
。有机物X的键线式为:

(1)有机物X的分子式___________________
(2)有机物Y是X的同分异构体,属于芳香烃,写出Y的结构简式 _______________________________________________________
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有_________种。
【答案】C8H8 ![]() 2
2
【解析】
(1)根据键线式的书写特点计算碳氢原子数;
(2)根据X的分子式为C8H8,结合苯环中碳原子数和氢原子数判断支链;
(3)X和氢气加成以后,所有的双键变为单键,根据对称性原则,这样得到的烃中被加成以后上去的氢原子均等效,共有两种类型的氢原子。
(1) 分子中含有8个碳原子和8个氢原子,其分子式为C8H8,
分子中含有8个碳原子和8个氢原子,其分子式为C8H8,
故答案为:C8H8;
(2) 的分子式为C8H8,Y中含有苯环,Y的支链含有2个碳原子和3个氢原子,则Y的结构简式:
的分子式为C8H8,Y中含有苯环,Y的支链含有2个碳原子和3个氢原子,则Y的结构简式:![]() ,
,
故答案为:![]() ;
;
(3)Z中心对称,并且镜面对称,所以角上一种,“Y“型交叉点一种,共有两种类型的氢原子,则Z的一氯代物有2种,
故答案为:2。

 活力课时同步练习册系列答案
活力课时同步练习册系列答案【题目】探究溶液酸碱性对![]() 溶液的配制和保存的影响。10mL
溶液的配制和保存的影响。10mL![]() 或10mL
或10mL![]() 溶液中。
溶液中。
I.![]() 溶液的配制
溶液的配制
将![]() 分别溶于10mL蒸馏水或10mL
分别溶于10mL蒸馏水或10mL
溶液编号 | 溶剂 | 溶液性状 | |
① | 蒸馏水 | 浅黄色澄清溶液: | 遇 |
② |
| 无色澄清溶液: | 遇 |
③ |
| 无色澄清溶液 | 遇 |
(1)用平衡移动原理解释①显酸性的主要原因是________________
(2)②、③变红发生反应的离子方程式是_______________________
(3)甲同学认为①中一定有+3价铁。他用激光笔照射“溶液”,观察到光路:又向含有KSCN的①中滴入试剂a,溶液变红,说明其推断正确,试剂a是____________
II ![]() 溶液的保存
溶液的保存
将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
溶液编号 | 溶液性状 | |
① | 橙色浑浊 | 用 |
② | 无色溶液 | 滴加5滴 |
③ | 无色溶液 | 滴加5滴 |
(分析讨论)①②说明酸性减弱时,![]() 溶液更易变质;②③说明……
溶液更易变质;②③说明……
(查阅资料)在一定pH范围内,+2价铁的还原性随酸性减弱而增强,氧气的氧化性随酸性的增强而增强。
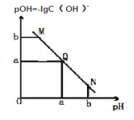
(进行实验)用右图所示装置完成实验(滴加试剂时溶液体积和溶液导电性变化可忽略)。向右池持续稳定通人氧气,待电流表示数稳定后:
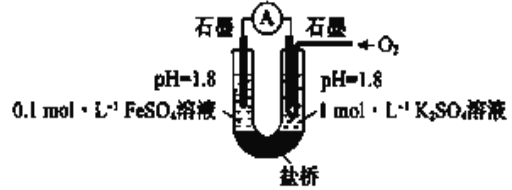
I 向左池滴加浓硫酸至![]() 接近
接近![]() ,电流没有明显变化
,电流没有明显变化
II 向右池滴加等量浓硫酸,电流明显增大。
(4)补全(分析讨论):②③说明_______________
(5)ii中右池的电极反应方程式是____________________
(6)依据实验推断:③比②中![]() 更易变质的原因是___________________
更易变质的原因是___________________
(7)按上述原理及装置重新进行实验证实①中![]() 更易变质的原因。实验方案及预期现象是:向右池持续稳定通人氧气,待电流计示数稳定后,____________
更易变质的原因。实验方案及预期现象是:向右池持续稳定通人氧气,待电流计示数稳定后,____________
(8)依据实验,配制并保存![]() 溶液的最佳法是_________________。
溶液的最佳法是_________________。
【题目】下列指定反应的化学用语表达正确的是( )
A | Mg(HCO3)2溶液与足量的NaOH溶液反应 | Mg2++2HCO |
B | 过量SO2通入到NaClO溶液中: | SO2+H2O+ClO-===HClO+ |
C | 向Al2(SO4)3溶液中加入过量的稀氨水 | Al3 ++4NH3·H2O=AlO2—+4NH4++2H2O |
D | KClO碱性溶液与Fe(OH)3反应制取K2FeO4 | 3ClO﹣+2Fe(OH)3=2FeO42﹣+3Cl﹣+4H++H2O |
A. AB. BC. CD. D