��Ŀ����
�����ڵ�����Ԫ��X��Y��Z��ԭ���������α�С��ԭ�Ӻ�����Ӳ���֮����5��XԪ��ԭ��������Ӳ��ϵĵ�������Y��Z��Ԫ��ԭ��������Ӳ��ϵĵ��������ܺͣ�YԪ��ԭ�ӵ�������Ӳ��ϵĵ����������ĵ��Ӳ�����2����XԪ���γ��⻯�������������ˮ�����ܷ�����Ӧ����ش�
��1��XԪ�������ڱ��е�λ�� ��XԪ���γ��⻯�������������ˮ�����ܷ�����Ӧ�Ļ�ѧ����ʽ ��
��2��Y�����������Ľṹʽ�� ��
��3��XZ3ʵ�����Ʒ��Ļ�ѧ����ʽΪ ��
��4��Z�ļ����������� ���塣������ӡ���ԭ�ӡ���
��1����2���ڵ�VA�壨���ڡ����1�֣�NH3+HNO3=NH4NO3
��2��O=C=O
��3��2 NH4Cl+Ca(OH)2 Ca Cl2+2 NH3��+2H2O
Ca Cl2+2 NH3��+2H2O
��4������
���������������1��ԭ�Ӻ�����Ӳ���֮����5��˵������Ԫ���в����ڵ�������Ԫ�أ�YԪ��ԭ�ӵ�������Ӳ��ϵĵ����������ĵ��Ӳ�����2��������Y��������������4��YΪCԪ�أ�X��ԭ����������Y���ڵڶ����ڣ�XԪ���γ��⻯�������������ˮ�����ܷ�����Ӧ������XΪNԪ�أ�λ��Ԫ�����ڱ��ĵ�2���ڵ�VA�壻XԪ���γ��⻯��NH3������������ˮ����HNO3�ܷ�����Ӧ�Ļ�ѧ����ʽNH3+HNO3=NH4NO3
��2��Y�����������Ϊ������̼��������C��O��˫����ϣ���ṹʽΪO=C=O��
��3��Zֻ���ǵ�һ����Ԫ����Ԫ�أ�XZ3��NH3ʵ�����Ʒ��Ļ�ѧ����ʽΪ2 NH4Cl+Ca(OH)2=" Ca" Cl2+2 NH3��+2H2O
��4��Z�ļ�������H2O���ڷ��Ӿ���
���㣺����Ԫ���ƶϣ��ṹʽ����ѧ����ʽ����д���������͵��ж�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�I����������߿���ÿһ�С�ÿһ���൱�����ڱ���ÿһ���ÿһ���ڣ�����������������������Ԫ�����ڱ���������������߿�����ʵ�������ڱ���1����6���ڵ�������������������ǽ����ķֽ��ߡ�
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | | | |
II��X��Y��Z��M��NΪ�����ڵ���������Ԫ�أ�����X��Zͬ���壬Y��Zͬ���ڣ�M��X��Y�Ȳ�ͬ���ڣ�Ҳ��ͬ�塣Xԭ�������������Ǻ�����Ӳ�����������Y���������ͼ۵Ĵ����͵���6��N�Ƕ���������Ԫ����ԭ�Ӱ뾶���ķǽ���Ԫ�ء�
��1��XԪ��λ��Ԫ�����ڱ��� ���ڣ��� �壻
NԪ��λ��Ԫ�����ڱ��� ���ڣ��� �塣
��2����д�����з�Ӧ�����ӷ���ʽ��
N����������������Һ��Ӧ��
��3��Y��Z��ȣ��ǽ����Խ�ǿԪ�ص�ԭ�ӽṹʾ��ͼΪ ������֤���ý��۵�ʵ���ǣ������ӷ���ʽ��ʾ��
��4���뽫X��Z��M��NԪ��ԭ�Ӱ뾶�Ӵ�С����
���ֶ�����Ԫ�ص����ʻ�ṹ��Ϣ���±����������Ϣ�ش��������⡣
| Ԫ�� | A | B | C | D |
| ���ʽṹ��Ϣ | ԭ��������������Ϊ���Ӳ�����2����������Ϊ����ɫ���壬��ȼ����ΪQ KJ/mol | ���ʳ��¡���ѹ�������壬������ˮ��ԭ�ӵ�M��p�����1��δ�ɶԵĵ��� | ��������������ɫ���塢������ǿ�������ڿ�����ȼ�շ�����ɫ�Ļ��档 | ԭ���������Ӳ���s����������p��������������һ����Ҫ�İ뵼����ϡ� |
��1��д��A��ȼ���ȷ���ʽ ��
��2��д��B������ˮ��Ӧ�Ļ�ѧ����ʽ ��
��3�����B��C�Ļ�����ˮ��Һ����Ҫ��ѧ���գ�д�����ӷ���ʽ ��
��4��A��C�γɵĻ�������ڵĻ�ѧ��Ϊ (����ۼ��������Ӽ���)��
��5��A��B��D����Ԫ�ص縺����С�����˳��Ϊ (дԪ�ط���)��
��6��B��D��Ԫ�طǽ����Խ������� (дԪ�ط���)�������һ��ʵ��֤����һ����: ��
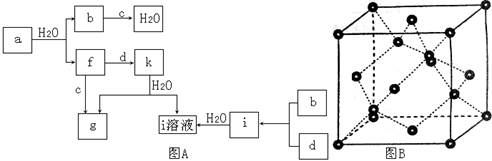

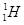 ��
��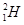 ��
��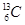 ��
��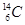 ��
��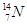 ��
��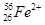 ��
��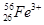 ��
��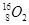 ��
��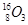 ����Ҫ��������¸��⣺
����Ҫ��������¸��⣺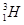 �ֱ�����Ԫ�ص�һ�� �����ǻ���Ϊ ��
�ֱ�����Ԫ�ص�һ�� �����ǻ���Ϊ ��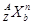 ��������Ҫ�����һ��(Ҫ��ÿС��ֱ�д������������������ӣ��Ҵ�������������ѡ��)��
��������Ҫ�����һ��(Ҫ��ÿС��ֱ�д������������������ӣ��Ҵ�������������ѡ��)��