题目内容
10.元素X原子的最外层有1个电子,元素Y原子的最外层有6个电子,这两种元素形成的化合物( )| A. | 只能是离子化合物X2Y | |
| B. | 只能是共价化合物X2Y2 | |
| C. | 既可能是离子化合物也可能是共价化合物 | |
| D. | 形成的化合物无论是X2Y还是X2Y2 原子都达到了8电子稳定结构 |
分析 X元素的原子最外层有1个电子,处于IA则,Y元素的原子最外层有6个电子,处于ⅥA族,可以形成H2O、Na2O、H2O2、Na2O2等化合物,据此分析解答.
解答 解:X元素的原子最外层有1个电子,处于IA则,Y元素的原子最外层有6个电子,处于ⅥA族,可以形成H2O、Na2O、H2O2、Na2O2等化合物.
A.可以形成Na2O2等离子化合物,故A错误;
B.可以形成H2O2等共价化合物,故B错误;
C.H2O、H2O2等为共价化合物,Na2O、Na2O2等为离子化合物,故C正确;
D.H2O、H2O2等为共价化合物,含有H元素,一定不满足8电子结构,故D错误,
故选C.
点评 本题考查原子结构与元素性质,难度不大,判断元素所处主族,再结合常见元素化合物进行解答,注意列举法的应用.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
1.保护环境已成为人类的共识,人类应以可持续发展的方式使用资源,以合理的方式对废物进行处理并循环使用.下列做法不利于环境保护的是( )
| A. | 引进电动汽车,减少汽车尾气排放 | |
| B. | 大力发展火电,缓解用电紧张 | |
| C. | 开发太阳能、风能、氢能等清洁能源 | |
| D. | 积极推行和使用能被微生物降解的新型聚合物材料 |
18.关于化学反应中的能量变化,下列说法中不正确的是( )
| A. | 燃烧反应都是放热反应 | |
| B. | 对于可逆反应:aA(g)+bB(g)?bC(g)+dD(g),如果正反应放热,逆反应一定吸热 | |
| C. | 氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量 | |
| D. | 只有放热的氧化还原反应才可以设计为原电池 |
5.下列关于中和热的说法不正确的是( )
| A. | 酸和碱发生中和反应时放出的热量不一定是57.3KJ | |
| B. | 酸和碱发生中和反应时所放出的热量就叫中和热 | |
| C. | 在稀溶液中,酸跟碱发生中和反应生成1mol水时所放出的热量称为中和热 | |
| D. | 中和热不包括物质溶解、电离、水合等过程中的热效应 |
15.一定温度下的恒容密闭容器中,可逆反应2NO2(g)?2NO(g)+O2(g)达到平衡状态的标志是( )
①2V(O2)=V(NO2)
②单位时间内生成n molO2的同时生成2n molNO2
③NO2、NO、O2的浓度之比为2:2:1
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变.
①2V(O2)=V(NO2)
②单位时间内生成n molO2的同时生成2n molNO2
③NO2、NO、O2的浓度之比为2:2:1
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变.
| A. | ②④⑥ | B. | ①④⑥ | C. | ②④⑤ | D. | 全部 |
2.若溶液中由水电离产生的c(OH-)=1×10-14 mol•L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
| A. | CH3COO- Na+ NO3- Cl- | B. | K+ Na+ Cl- NO3- | ||
| C. | K+ Na+ Cl- AlO2- | D. | K+ I- SO42- NO3- |
 硼(B)及其化合物在化学中有重要的地位.请回答下列问题:
硼(B)及其化合物在化学中有重要的地位.请回答下列问题: [B(OH)4]-+H+.
[B(OH)4]-+H+.
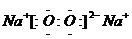 ;所含化学键类型为离子键、共价键(或离子键、非极性键);A晶体的晶胞中阳离子和阴离子的个数比为2:1.
;所含化学键类型为离子键、共价键(或离子键、非极性键);A晶体的晶胞中阳离子和阴离子的个数比为2:1. .
.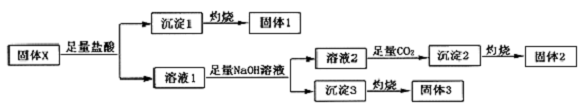
 ,沉淀2的化学式为Al(OH)3.
,沉淀2的化学式为Al(OH)3.