题目内容
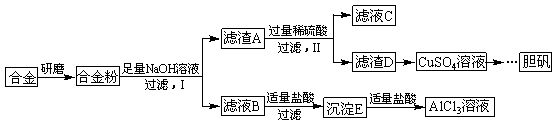
铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。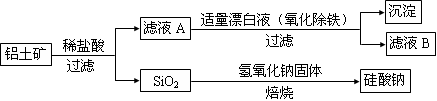
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的方法为: (注明试剂、现象)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为 (填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、冷却结晶、 (填操作名称)、洗涤。
④该过程中涉及某氧化还原反应如下,请完成:
□Fe2++ □ClO-+ □ = □Fe(OH)3↓+ □C1-+ □ 。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号)。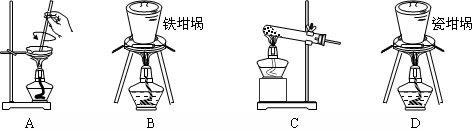
(1)①取少量滤液B,加入KSCN溶液,若不变红,再加入氯水,仍然不变红,说明滤液B中不含铁元素。(其他合理答案均得分)
②c ③过滤 ④2、1、5H2O 、2、1、4H+(2)B
解析试题分析:(1)①溶液中铁的存在形态是铁离子或亚铁离子,铁离子和KSCN溶液反应显红色。亚铁离子具有还原性,据此可以检验铁元素的存在。即取少量滤液B,加入KSCN溶液,若不变红,再加入氯水,仍然不变红,说明滤液B中不含铁元素。
②滤液B中铝元素以铝离子的形成存在,因此要生成氢氧化铝白色沉淀,需要加入碱液。由于氢氧化铝是两性氢氧化物,能溶解在强碱溶液中,所以最好选择的试剂是氨水,答案选c。
③晶体从溶液中析出后,要从溶液中分离出来,需要利用过滤操作完成分离。
④在反应中亚铁离子失去1个电子,氯元素的化合价从+1价降低到-1价,得到2个电子。根据电子得失守恒可知,还原剂亚铁离子与氧化剂ClO-的物质的量之比是2:1。根据电荷守恒可知,反应物还有水参加,而生成物中还有氢离子生成,所以配平后的离子方程式为2Fe2++ClO-+5H2O=2Fe(OH)3↓+ C1-+4H+。
(2)固体灼烧需要坩埚,由于瓷坩埚中还有二氧化硅,在高温下与氢氧化钠反应,要从选择铁坩埚,答案选B。
考点:考查铁离子、亚铁离子检验、氢氧化铝的制备、过滤、氧化还原反应的配平以及二氧化硅的性质等

(14分)甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。
| 操 作 | 现 象 |
通入氯气至过量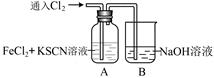 | I.A中溶液变红 II.稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是______。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在_______。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象II的原因是SCN—与Cl2发生了反应。
(4)甲同学猜想SCN—可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN—的电子式为
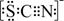 。
。①甲同学认为SCN—中碳元素没有被氧化,理由是______。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN—中被氧化的元素是______。
③通过实验证明了SCN—中氮元素转化为,他的实验方案是______。
④若SCN—与Cl2反应生成1 mol CO2,则转移电子的物质的量是______mol。


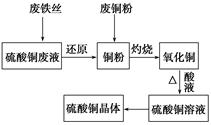
 8Cu+4FeO+2Fe2O3+16SO2反应制取铜及其硫和铁的化合物。
8Cu+4FeO+2Fe2O3+16SO2反应制取铜及其硫和铁的化合物。