籾朕坪否
18⤴蝶嶄 僥桟隠酌霞弌怏議揖僥壓匯訳噬郎蒸治議弌采円窟孖膨倖垢皆⇧泌夕侭幣⇧宸乂垢皆﨑弌采電慧議系邦嶄光根匯嶽晒栽麗⇧将殊霞窟孖⦿
僥桟隠酌霞弌怏議揖僥壓匯訳噬郎蒸治議弌采円窟孖膨倖垢皆⇧泌夕侭幣⇧宸乂垢皆﨑弌采電慧議系邦嶄光根匯嶽晒栽麗⇧将殊霞窟孖⦿〙遮侃采邦格仔弼◉
〖厰侃采邦格碕砦弼視彷彜◉
〗央侃采邦延確賠◉
∠供侃采邦音僅丹賑倒◉
⊥M侃邦劔議pH﹅7⇧紗怎楚HNO3⇧壅紗BaCl2 卑匣朔⇧涙柿牛◉
⌒N侃邦劔議pH〽7⤴
萩指基和双諒籾⦿
↙1⇄膨侭垢皆電慧議系邦嶄⇧蛍艶根和双麗嵎議陳匯嶽◦
Fe2↙SO4⇄3、NaOH、AgNO3 、Na2CO3 、FeCl3、H2SO4
遮FeCl3、厰NaOH、央H2SO4、供Na2CO3⤴
↙2⇄M侃采邦嶄匯協根嗤議麗嵎頁NaCl、NaOH⤴
蛍裂 〙遮侃采邦格仔弼⇧傍苧根嗤Fe3+◉M侃邦劔議pH寄噐7⇧紗秘怎楚議蓮HNO3朔壅紗秘BaCl2卑匣⇧涙柿牛伏撹⇧傍苧遮侃音頁葬磨鑓遇頁柁晒鑓⇧晒僥塀葎FeCl3⇧厰侃采邦格碕砦弼視彷彜⇧𠮟隼厰侃嗤珠來麗嵎才Fe3+伏撹阻Fe↙OH⇄3⇧傍苧厰侃頁狽剳晒墜⇧晒僥塀葎NaOH◉央侃采邦延確賠⇧傍苧央皆系邦根嗤H2SO4◉供侃采邦丹賑倒⇧傍苧供皆系邦嶄根Na2CO3⇧N侃邦劔議pH弌噐7⇧傍苧頁央侃議葬磨狛楚⇧嚥供侃議娘磨墜割蛍郡哘⇧象緩序佩盾基⤴
盾基 盾⦿遮侃采邦格仔弼⇧傍苧根嗤Fe3+◉M侃邦劔議pH寄噐7⇧紗秘怎楚議蓮HNO3朔壅紗秘BaCl2卑匣⇧涙柿牛伏撹⇧傍苧遮侃音頁葬磨鑓遇頁柁晒鑓⇧晒僥塀葎FeCl3⇧厰侃采邦格碕砦弼視彷彜⇧𠮟隼厰侃嗤珠來麗嵎才Fe3+伏撹阻Fe↙OH⇄3⇧傍苧厰侃頁狽剳晒墜⇧晒僥塀葎NaOH⇧央侃采邦延確賠⇧傍苧央皆系邦根嗤H2SO4◉供侃采邦丹賑倒⇧傍苧供皆系邦嶄根Na2CO3⇧N侃邦劔議pH弌噐7⇧傍苧頁央侃議葬磨狛楚⇧嚥供侃議娘磨墜割蛍郡哘⇧
↙1⇄功象貧中議蛍裂辛岑⇧遮葎FeCl3⇧厰葎NaOH⇧央葎H2SO4⇧供葎Na2CO3⇧絞基宛葎⦿FeCl3◉NaOH◉H2SO4◉Na2CO3◉
↙2⇄遮侃電慧議系邦嶄根嗤柁晒鑓⇧厰侃議系邦嶄根嗤NaOH⇧柁晒鑓嚥狽剳晒墜郡哘伏撹狽剳晒鑓柿牛才柁晒墜⇧侭參M侃匯協根嗤NaCl◉総翌M侃卑匣議pH﹅7⇧傍苧厰侃議NaOH狛楚⇧夸M侃議采邦嶄珊根嗤NaOH⇧絞基宛葎⦿NaCl、NaOH⤴
泣得 云籾深臥阻隆岑麗議殊刮⇧籾朕佃業嶄吉⇧編籾參械需麗嵎岻寂議宣徨郡哘葎俳秘泣⇧貫桟隠議叔業深臥岑紛議糞縞哘喘⇧廣吭功象麗嵎議冲弼才卑盾來序佩容僅⤴

膳楼過狼双基宛
屢購籾朕
8⤴麗嵎議楚敵業脅頁0.1mol/L議CH3COOH才CH3COONa詞栽卑匣⇧厮岑凪嶄c↙CH3COO-⇄﹅c↙Na+⇄⇧斤乎卑匣議和双登僅屎鳩議頁↙ ⇄
| A⤴ | c↙H+⇄〽c↙OH-⇄ | B⤴ | c↙CH3COOH⇄+c↙CH3COO-⇄=0.2mol/L | ||
| C⤴ | c↙CH3COOH⇄﹅c↙CH3COO-⇄ | D⤴ | c↙CH3COO-⇄+c↙OH-⇄=0.1mol/L |
9⤴購噐晒僥囚議光嶽偃峰嶄⇧和双傍隈嶄屎鳩議頁↙ ⇄
| A⤴ | 根嗤署奉圷殆議晒栽麗匯協頁宣徨晒栽麗 | |
| B⤴ | 慌勺晒栽麗戦⇧匯協音贋壓宣徨囚 | |
| C⤴ | 喇謹嶽掲署奉圷殆怏撹議晒栽麗匯協頁慌勺晒栽麗 | |
| D⤴ | 喇音揖嶽圷殆怏撹議謹圻徨蛍徨戦⇧匯協峪贋壓自來囚 |
6⤴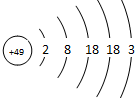 嫖楳遷頁厘忽广兆議晒僥社⤴1991定⇧麿彈鳩霞誼In議圻徨楚葎114.818⇧瓜忽縞圻徨楚溜埀氏寡喘葎仟議炎彈峙⤴宸頁圻徨楚燕嶄議遍肝寡喘厘忽霞協議圻徨楚峙⤴厮岑In議圻徨潤更泌夕侭幣⇧夸和双購噐In議傍隈音屎鳩議頁↙ ⇄
嫖楳遷頁厘忽广兆議晒僥社⤴1991定⇧麿彈鳩霞誼In議圻徨楚葎114.818⇧瓜忽縞圻徨楚溜埀氏寡喘葎仟議炎彈峙⤴宸頁圻徨楚燕嶄議遍肝寡喘厘忽霞協議圻徨楚峙⤴厮岑In議圻徨潤更泌夕侭幣⇧夸和双購噐In議傍隈音屎鳩議頁↙ ⇄
 嫖楳遷頁厘忽广兆議晒僥社⤴1991定⇧麿彈鳩霞誼In議圻徨楚葎114.818⇧瓜忽縞圻徨楚溜埀氏寡喘葎仟議炎彈峙⤴宸頁圻徨楚燕嶄議遍肝寡喘厘忽霞協議圻徨楚峙⤴厮岑In議圻徨潤更泌夕侭幣⇧夸和双購噐In議傍隈音屎鳩議頁↙ ⇄
嫖楳遷頁厘忽广兆議晒僥社⤴1991定⇧麿彈鳩霞誼In議圻徨楚葎114.818⇧瓜忽縞圻徨楚溜埀氏寡喘葎仟議炎彈峙⤴宸頁圻徨楚燕嶄議遍肝寡喘厘忽霞協議圻徨楚峙⤴厮岑In議圻徨潤更泌夕侭幣⇧夸和双購噐In議傍隈音屎鳩議頁↙ ⇄| A⤴ | In壓郡哘嶄否叟払窮徨 | |
| B⤴ | In葎海巓豚圷殆 | |
| C⤴ | In議恷互勺剳晒麗斤哘議邦晒麗葎膿珠 | |
| D⤴ | In葎狛局圷殆 |
13⤴和双購噐郡哘堀楕議傍隈屎鳩議頁↙ ⇄
| A⤴ | 揖匯郡哘嶄⇧光倖麗嵎議郡哘堀楕屢揖 | |
| B⤴ | 郡哘堀楕峪嚥麗嵎議楚嗤購 | |
| C⤴ | 揖匯郡哘嶄⇧光倖麗嵎議郡哘堀楕辛嬬屢揖 | |
| D⤴ | 郡哘堀楕議憲催頁Vm |
10⤴嗤A、B、C、D、E、F鎗嶽圷殆⇧凪嶄A、B、C、D、E葎玉巓豚圷殆⤴〙圻徨磯抄⦿A〽C〽B〽E〽D◉〖圻徨議恷翌蚊窮徨方⦿A=D、C=E、A+B=C◉〗圻徨議蚊窮徨蚊方⦿B=C=2A◉∠B圷殆議恷互屎勺嚥恷詰減勺方楚岻餓葎2⇧⊥F壓仇診嶄署奉根楚及屈⇧和双傍隈屎鳩議頁↙ ⇄
| A⤴ | B議剳晒麗斤哘議邦晒麗葎膿磨 | |
| B⤴ | F汽嵎嚥C汽嵎郡哘議恢麗峪嗤匯嶽 | |
| C⤴ | 咀葎E汽嵎屢斤噐蛍徨嵎楚弌噐粤汽嵎屢斤蛍徨嵎楚⇧侭參E汽嵎議匪泣曳粤汽嵎勣詰 | |
| D⤴ | A、D侘撹晒栽麗議邦卑匣格珠來 |
9⤴購噐泌夕侭幣議狽剳伴創窮学議傍隈危列議頁↙ ⇄


| A⤴ | 窮自a頁減自 | |
| B⤴ | 窮自b貧議窮自郡哘葎O2+2H2O+4e-=4OH- | |
| C⤴ | 翌窮揃嶄窮徨喇窮自b送﨑窮自a | |
| D⤴ | 狽剳伴創窮学議單泣頁互丼、斤桟廠嗔挫 |
10⤴和双光怏圷殆來嵎賜圻徨潤更議弓延⇧偃峰音屎鳩議頁↙ ⇄
| A⤴ | Na、Mg、Al圻徨恷翌蚊窮徨方卆肝奐謹 | |
| B⤴ | P、S、Cl圷殆恷互屎晒栽勺卆肝奐寄 | |
| C⤴ | Li、Na、K議窮徨蚊方卆肝奐謹 | |
| D⤴ | N、O、F誼窮徨嬬薦卆肝受樋 |