题目内容
【题目】一氯甲烷(CH3Cl)是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等。
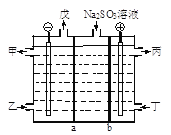
(1)甲组同学在实验室用下图所示装置模拟催化法制备和收集一氯甲烷。

①仪器a的名称为___________。
②无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为_____________。
③装置B的主要作用是_____________。
(2)乙组同学选用甲组A、B装置和下图所示的部分装置检验CH3Cl中的氯元素。
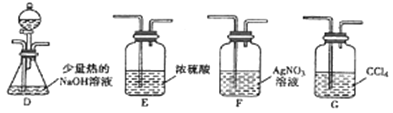
①乙组同学的实验装置中,依次连接的合理顺序为A→B→_____→_____→_____。
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞先后加入两种试剂,观察实验现象。分液漏斗中先后加入的试剂是_______________。
③能证明CH3Cl中含有氯元素的实验现象是____________。
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3Cl中的卤素原子。相关数据如下表:
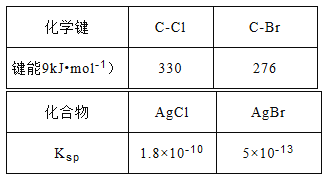
将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀。请依据表中数据解释原因__________________。
【答案】 圆底烧瓶 CH3OH+HCl(浓) ![]() CH3Cl+H2O 除去CH3OH蒸气、HCl等杂质气体 F D G 硝酸、硝酸银 C-Br键的键能小,更容易断裂 Ksp(AgBr)< Ksp(AgCl),AgBr更容易沉淀
CH3Cl+H2O 除去CH3OH蒸气、HCl等杂质气体 F D G 硝酸、硝酸银 C-Br键的键能小,更容易断裂 Ksp(AgBr)< Ksp(AgCl),AgBr更容易沉淀
【解析】(1)①根据仪器构造可知仪器a的名称为圆底烧瓶;②甲醇与浓盐酸在作催化剂的条件下发生取代反应生成一氯甲烷和水,反应的化学方程式为CH3OH+HCl(浓) ![]() CH3Cl+H2O;③氯化氢、甲醇均易挥发,所以要用水除去一氯甲烷中的氯化氢和甲醇蒸汽,所以装置B的主要作用是除去氯化氢气体和甲醇;(2)根据题意,检验CH3Cl中的氯元素,可以将一氯甲烷通入到热的氢氧化钠溶液中,反应一段时间后再加入用硝酸酸化的硝酸银溶液,根据是否有白色沉淀生成可判断氯元素的存在,①根据上面的分析可知,装置依次连接的合理顺序为A、B、F、D、G;②根据上面的分析可知,分液漏斗中盛放的试剂是硝酸、硝酸银,故答案为:硝酸、硝酸银;③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成;(3)依据表中数据可知,C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀,所以先出现淡黄色溴化银沉淀。
CH3Cl+H2O;③氯化氢、甲醇均易挥发,所以要用水除去一氯甲烷中的氯化氢和甲醇蒸汽,所以装置B的主要作用是除去氯化氢气体和甲醇;(2)根据题意,检验CH3Cl中的氯元素,可以将一氯甲烷通入到热的氢氧化钠溶液中,反应一段时间后再加入用硝酸酸化的硝酸银溶液,根据是否有白色沉淀生成可判断氯元素的存在,①根据上面的分析可知,装置依次连接的合理顺序为A、B、F、D、G;②根据上面的分析可知,分液漏斗中盛放的试剂是硝酸、硝酸银,故答案为:硝酸、硝酸银;③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成;(3)依据表中数据可知,C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀,所以先出现淡黄色溴化银沉淀。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案