题目内容
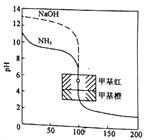
【题目】室温下,用相同浓度的NaOH溶液,分别滴定100mL浓度均为O.1mol/L的三种酸(HM、HN和HR)溶液,滴定的曲线如图所示,下列判断错误的是

A. 三种酸的电离常数关系:KHM>KHN>KHR
B. pH=7时,三种溶液中:c(M-)>c(N-)>c(R-)
C. 当中和百分数达100%时,将三种溶液混合后:c(HM)+c(HN)+c(HR)=c(OH-)-c(H+)
D. 滴定至P点时,溶液中:c(HN)>c(N-)>c(Na+)>c(H+)>c(OH-)
【答案】D
【解析】A.根据图像,0.1mol·L-1的三种酸(HM、HN和HR)溶液的起始pH中HM最小,酸性最强,HR的pH最大,酸性最弱,酸性越强,电离平衡常数越大,三种酸的电离常数关系:KHM>KHN>KHR,A正确;B.pH=7时,三种溶液中阴离子的水解程度不同,加入的氢氧化钠的体积不同,三种离子浓度分别与钠离子浓度相等,但三种溶液中钠离子浓度不等,其中HR需要的氢氧化钠最少,所以三种溶液中:c(M-)>c(N-)>c(R-),B正确;C.此为混合溶液的质子守恒关系式,c(HM)+c(HN)+c(HR)=c(OH-)-c(H+),C正确;D.滴定至P点时溶质为等物质的量浓度的HN和NaN,溶液显酸性,HN的电离为主,但电离程度较小,因此c(N-)>c(Na+)>c(HN)>c(H+)>c(OH-) ,D错误;答案选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容。
用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度如表所示:
N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度如表所示:
时间/t | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
(1)10~20 min内,NO的平均反应速率![]() (NO)=______________,T1℃时,该反应的平衡常数K=___________________。
(NO)=______________,T1℃时,该反应的平衡常数K=___________________。
(2)30min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是_______(填写相应的字母)。
a.通入一定量的NO b.加入一定量的C
c.适当升高反应体系的温度 d.加入合适的催化剂
(3)若保持与上述反应前30min的反应条件相同,起始时NO的浓度为2.50mol·L-1,则反应达平衡时c(NO)=_________mol·L-1,NO的转化率__________(填“增大”、“减小”或“不变”)。