题目内容
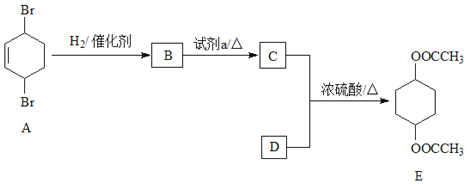
【题目】碳及其化合物广泛存在于自然界中。回答下列问题:
(1)在基态14C原子中,核外存在______对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是__________。
(3)CS2分子中,共价键的类型有________,C原子的杂化轨道类型是______,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______。
(4)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:
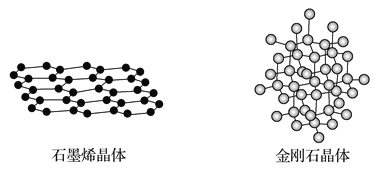
①在石墨烯晶体中,每个C原子连接_____个六元环,每个六元环占有___个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接_____个六元环,六元环中最多有______个C原子在同一平面。
【答案】2 C有4个价电子且半径小,难以通过得或失电子达到稳定电子结构 σ键和π键 sp CO2、SCN-(或COS等,) 3 2 12 4
【解析】
(1)根据同一轨道的2两个电子自旋方向相反判断;
(2)共价键为原子之间以共用电子对成键,碳原子有4个价电子,且半径较小,反应中难以失去或得到电子;
(3)CS2分子的结构式为S=C=S,含有σ键和π键;结合σ键和孤对电子数判断价层电子对数,以此判断杂化类型;根据等电子体进行判断;
(4)石墨晶体中最小的环为六元环,每个碳原子形成3个C-C键,每个C-C键被2个碳原子共用;在金刚石晶体中,每个C原子与周围的4个碳原子形成四个碳碳单键,最小的环为六元环,每个单键为三个环共有。
(1)基态C原子核外电子排布式为1s22s22p2,轨道排布式为:![]() ,则在基态14C原子中,核外存在2对自旋相反的电子;
,则在基态14C原子中,核外存在2对自旋相反的电子;
(2)共价键为原子之间以共用电子对成键,碳原子有4个价电子,且半径较小,反应中难以失去或得到电子,故碳在形成化合物时,其键型以共价键为主;
故答案为:C有4个价电子且半径小,难以通过得或失电子达到稳定电子结构;
(3)CS2分子的结构式为S=C=S,含有σ键和π键,CS2分子中C原子形成2个σ键,孤对电子数为![]() =0,则C为sp杂化;
=0,则C为sp杂化;
O与S同主族,所以与CS2具有相同空间构型和键合形式的分子为CO2或COS等;与CO2互为等电子体的离子有SCN-,所以SCN-的空间构型与CS2键合方式与相同;
(4)①石墨晶体中最小的环为六元环,每个碳原子形成3个C-C键,则每个C原子连接 3个六元环,每个六元环占有的C原子数为6×![]() =2;
=2;
②在金刚石晶体中,每个C原子与周围的4个碳原子形成四个碳碳单键,最小的环为六元环,每个单键为三个环共有,则每个C原子连接4![]() 3=12个六元环,晶胞中共平面的原子如图
3=12个六元环,晶胞中共平面的原子如图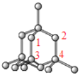 ,共4个。
,共4个。

【题目】利用如图所示的装置研究SO2的性质:
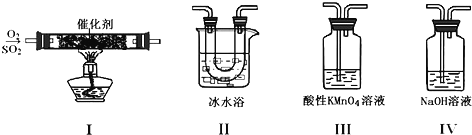
已知:
物质 | 熔点℃ | 沸点℃ |
SO2 | -76.1 | -10 |
SO3 | 16.8 | 45 |
(1)装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式________________。
(2)甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是___;观察到装置Ⅲ中现象是________________,说明二氧化硫具有___性
(3)乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置(装置Ⅱ中充分冷却),若装置Ⅳ中有40mL2.5mol/LNaOH溶液,反应后增重4.8g,则装置Ⅳ中发生反应的总的化学方程式是___
【题目】为验证氧化性:Cl2>Fe3+>SO2,某化学研究性学习小组用如图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕):
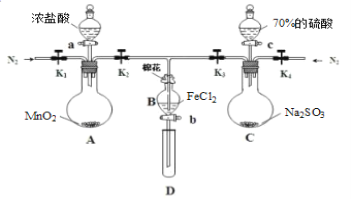
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是_____________。
(2)棉花中浸润的溶液为________________,作用是____________ 。
(3)导致步骤Ⅲ中溶液变黄的离子反应是__________,用________(写试剂化学式)检验氧化产物,现象是____________。
(4)能说明氧化性Fe3+>SO2的离子方程式是___________。
(5)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性:Cl2>Fe3+>SO2的是_______(填“甲”“乙”“丙”)。
过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
甲 | 有Fe3+无Fe2+ | 有 |
乙 | 既有Fe3+又有Fe2+ | 有 |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |