题目内容
【题目】氢叠氮酸(HN3)及其盐(如NaN3、NH4N3、CuN3等)都具有爆炸性,最近南京理工大学胡丙成教授团队成功合成出PHAC,其化学式为(N3)6(H3O)3(NH4)4Cl。回答下列问题:
(1)PHAC中“N3”的化合价为______。N2F2的电子式为_______。
(2)汽车安全气囊中的NaN3可发生下列反应:
NaN3(s)=Na(s)+3/2N2(g) △H1;
2NaN3(s)+CuO(s)=Na2O(s)+3N2(g)+Cu(s) △H1;
则反应CuO(s)+2Na(s)=Na2O(s)+Cu(s) △H=_______(用△H1和△H2表示)
(3)25℃时,将lmolNH4N3投入一2L的恒容密闭容器中,0.5min后反应达到平衡,测得生成的两种单质的物质的量之和为1.6mol, 则NH4N3的平衡转化率为_______,25℃时该反应的平衡常数K=________。
(4)氢叠氮酸(HN3)易溶于水,且酸性与醋酸相近。
①HN3在水溶液中的电离方程式为_______________.
② 0.1mol/L的HN3溶液与0.1mol/L的NaN3等体积混合,混合溶液中各离子浓度由大到小的顺序为__________________。
③ 已知T℃时,Ksp(CuN3)=5.0×10-9,Ksp(Cu2S)=2.5×10-48,则相同温度下反应:
Cu2S(s)+2N3-(aq)![]() 2CuN3(s)+S2-(aq)的平衡常数K=_________.
2CuN3(s)+S2-(aq)的平衡常数K=_________.
【答案】 –l ![]() △H2-2△H1 40% 0.0256 HN3
△H2-2△H1 40% 0.0256 HN3![]() H++N3- c(N3-)>c(Na+)>c(H+)>c(OH-) 1.0×10-31
H++N3- c(N3-)>c(Na+)>c(H+)>c(OH-) 1.0×10-31
【解析】(1)根据正负价代数和为0可知PHAC中“N3”的化合价为-价。根据8电子稳定结构可知N2F2的电子式为![]() 。(2)已知:
。(2)已知:
①NaN3(s)=Na(s)+3/2N2(g) △H1;
②2NaN3(s)+CuO(s)=Na2O(s)+3N2(g)+Cu(s) △H1;
则根据盖斯定律可知②-①×2即得到反应CuO(s)+2Na(s)=Na2O(s)+Cu(s) △H=△H2-2△H1。
(3)根据反应的方程式可知
NH4N3=2H2↑+2N2↑
起始浓度(mol/L) 0.5 0 0
转化浓度(mol/L) x 2x 2x
平衡浓度(mol/L) 0.5-x 2x 2x
则2x+2x=1.6/2,解得x=0.2
因此NH4N3的平衡转化率为0.2/0.5×100%=40%,25℃时该反应的平衡常数K=![]() 。
。
(4)①氢叠氮酸(HN3)易溶于水,且酸性与醋酸相近,因此HN3在水溶液中的电离方程式为HN3![]() H++N3-。②由于酸性与醋酸相近,因此0.1mol/L的HN3溶液与0.1mol/L的NaN3等体积混合后显酸性,则混合溶液中各离子浓度由大到小的顺序为c(N3-)>c(Na+)>c(H+)>c(OH-)。③相同温度下反应Cu2S(s)+2N3-(aq)
H++N3-。②由于酸性与醋酸相近,因此0.1mol/L的HN3溶液与0.1mol/L的NaN3等体积混合后显酸性,则混合溶液中各离子浓度由大到小的顺序为c(N3-)>c(Na+)>c(H+)>c(OH-)。③相同温度下反应Cu2S(s)+2N3-(aq)![]() 2CuN3(s)+S2-(aq)的平衡常数K=
2CuN3(s)+S2-(aq)的平衡常数K=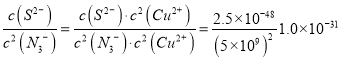 。
。

【题目】某研究小组在实验室进行硫的化合物系列实验。
Ⅰ.验证H2SO3的酸性比H2CO3强,甲同学设计下图装置。
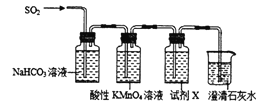
(1)试剂X的作用是_______。
(2)当观察到_______,即证明H2SO3的酸性比H2CO3强。
Ⅱ.研究铁与硫酸的反应。
已知: 浓H2SO4的沸点为338.2℃。
a.乙同学设计如下表所示的实验1、2:
实验 | 试剂 | 现象 | |
| 1 | 螺旋状铁丝、稀硫酸 | 铁丝表面有大量气体产生。 |
2 | 螺旋状铁丝、浓硫酸 | 铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止。 | |
(3)上述实验中,铁丝绕成螺旋状的目的是_______。
(4)实验1中,铁与稀硫酸反应的离子方程式为_______。
(5)实险2中的现象常被称为_______。
b.丙同学设计如图所示装置的实验3:
加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体,实验结束后,检验到A的溶液中既有Fe3+又有Fe2+。

(6)A中产生的气体是_______; 请设计实验方案检测装置A的溶液中含有Fe3+_______ (简要说明操作、试剂、现象和结论)。
(7)分析实验1、2、3,可知影响铁和硫酸反应产物多样性的因素有_______。