��Ŀ����
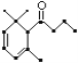
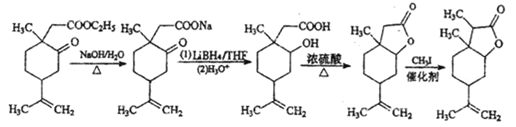
����Ŀ����ͼ��һ����Ȼҩ���Ż����ӺϳɵIJ���·��ͼ����Ӧ�����Ѿ���ȥ����
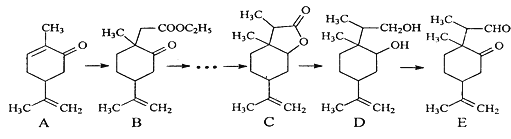
��֪����LiBH4�ɽ�ȩ��ͪ�����ԭ�ɴ��������ܻ�ԭ���ᡢ�����Ρ�̼̼˫����LiBH4�����ֽ⡣
��RCH2COOR' ![]() RCH(CH3)COOR'��RCOR'
RCH(CH3)COOR'��RCOR' ![]() RCH(OH)R'��RCOOR'
RCH(OH)R'��RCOOR' ![]() RCH2OH+R'OH��
RCH2OH+R'OH��
��1����ӦA��B����Ҫ�����Լ�X�������ʽΪC4H8O2��X�Ľṹ��ʽΪ_____��
��2��C��LiBH4��ԭ�õ�D��C��D��ֱ������������H2��ԭ��ԭ����______��
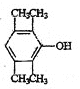
��3��д��һ����������������A��ͬ���칹��Ľṹ��ʽΪ_____________�������ڷ����廯�������ʹFeCl3��Һ��ɫ���۷�������4�ֲ�ͬ��ѧ�������⡣
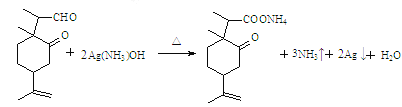
��4��д��E��������Һ��Ӧ�Ļ�ѧ����ʽ_________��
��5����������֪ʶ����������Ϣ�����B��C�ĺϳ�·��ͼ��CH3I�����Լ���ѡ�����ϳ�·�߳��õı�ʾ��ʽΪ��![]() ��____________
��____________
���𰸡�CH3COOC2H5 ����̼̼˫���������ӳɣ���ԭ���������Ѻ������ӳɣ���ԭ��  ��
��
��������
��1����ӦA��B����Ҫ�����Լ�X�������ʽΪC4H8O2�����ڼӳɷ�Ӧ����XΪCH3COOC2H5��
��2������̼̼˫����H2�ӳɻ�ԭ�������Ѻ�H2������ԭ��Ӧ��
(3)�����ڷ����廯���˵�����б���������ʹFeCl3��Һ��ɫ��˵�����з��ǻ����ۺ˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�ṹӦ�Գƣ�
��4��E��ȩ����������Һ����������Ӧ��
��5���Ƚ�B��C�Ľṹ��ʽ��֪��B�����������Ƶ�ˮ��Һ�з���ˮ�ⷴӦ�����������ƣ�Ȼ���ʻ���LiBH4��ԭΪ����Ȼ���ữ���������Ʊ�Ϊ�Ȼ����Ȼ����ǻ���Ũ���ᡢ���������·���ȡ����Ӧ�������������������CH3I��������Cԭ�ӵķ�Ӧ�õ�C��
��1������A��B�Ľṹ��ʽ����ͬ�����X�ķ���ʽ��֪��Aת��ΪB���ڼӳɷ�Ӧ����X��CH3COOC2H5��
��2��C��D��ֱ����H2(��������)��ԭ��ԭ���ǣ���ΪC�к���̼̼˫����̼̼˫��Ҳ�������������ӳɷ�Ӧ�������Ѻ�H2������ԭ��Ӧ��
�ʴ�Ϊ������̼̼˫���������ӳ�(��ԭ)�������Ѻ������ӳ�(��ԭ)��
(3)A��ͬ���칹�����㣺�����ڷ����廯���˵�����б���������ʹFeCl3��Һ��ɫ��˵�����з��ǻ����ۺ˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬A�ķ���ʽ��C10H14O��������д��ڶԳƽṹ�����Է��������A��ͬ���칹��Ľṹ��ʽ��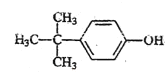 ��
�� ��
��
��4��E�����е�ȩ������������Һ��Ӧ��ȩ��������Ϊ�Ȼ���ͬʱ���ɰ����������ʡ�ˮ����ѧ����ʽ�� ��
��
��5���Ƚ�B��C�Ľṹ��ʽ��֪��B�����������Ƶ�ˮ��Һ�з���ˮ�ⷴӦ�����������ƣ�Ȼ���ʻ���LiBH4��ԭΪ����Ȼ���ữ���������Ʊ�Ϊ�Ȼ����Ȼ����ǻ���Ũ���ᡢ���������·���ȡ����Ӧ�������������������CH3I��������Cԭ�ӵķ�Ӧ�õ�C���ϳ�����ͼ�ǣ�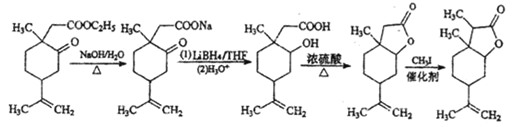 ��
��

����Ŀ��Cr��S��Ԫ�صĻ����ﳣ�����һЩ�������⣬���й����������о��ø��ֻ�ѧ������������Щ���ʶԻ�����Ӱ�졣
��1����ԭ�������Ǵ���������Cr2O72��CrO42����ҵ��ˮ�ij��÷������������£�
![]()
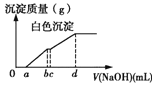
����֪�������£���ʼŨ��Ϊ1.0 mol��L1��Na2CrO4��Һ��c(Cr2O72)��c(H+)�ı仯��ͼ��ʾ��������������CrO42-ת��ΪCr2O72-�����ӷ���ʽΪ______________________��
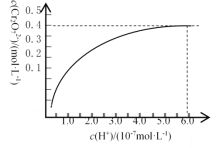
����ԭ�������������뻹ԭ�������ʵ���֮��Ϊ__________��
��Cr3+��Al3+�Ļ�ѧ�������ƣ���CrCl3��Һ���ɲ����գ����յõ��Ĺ���Ļ�ѧʽΪ____________��
�������£�Ksp[Cr(OH)3]=1.0��10-32����ʹ�������ˮ�е�c(Cr3+)����1.0��10-5mol��L1����������ȫ����Ӧ��������Һ��pH=_____��
��2�����������η����������е�SO2
��������ͨ��1.0mol/L ��Na2SO3��Һ����Na2SO3ǡ����ȫ��Ӧʱ����ҺpHԼΪ3����ʱ����Һ�и�������Ũ���ɴ�С��˳��Ϊ_________��������Ũ�ȷ��ź��������ű�ʾ����
�������£����̵���ͨ��(NH4)2SO3��Һ�У������ҺpH�뺬��������ʵ��������ı仯��ϵ��ͼ��ʾ��
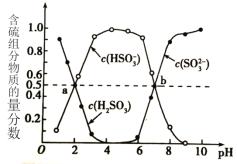
��֪����������ʵĵ��볣����25�棩���£�
����� | ���볣�� |
H2SO3 | Ka1=1.54��10-2 Ka2=1.02��10-7 |
NH3��H2O | Kb=1.74��10-5 |
��i��(NH4)2SO3��Һ��____�����������������������������ԣ���ԭ����_________________��
��ii��ͼ��b��ʱ��ҺpH=7����n(NH4+):n(HSO3- )=_________��