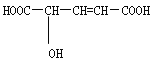题目内容
【题目】如图所示,淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应。A、B、C都可以被强还原剂还原成为D(C6H14O6)。已知,相关物质被氧化的难易次序是:RCHO最易,R—CH2OH次之,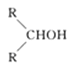 最难。
最难。
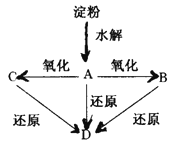
请回答下列问题:
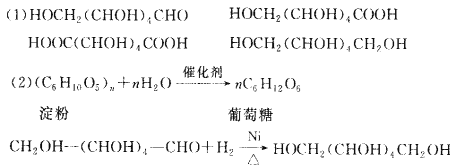
(1)请在下列横线上填写A、B、C、D的结构简式。
A: ;B: ;C: ;D: 。
(2)写出下列反应的化学方程式。
淀粉→A:
A→D:
【答案】
【解析】
试题分析:淀粉在催化剂(如酸)存在和加热条件下可以逐步水解,生成一系列比淀粉分子小的化合物,最后生成还原性的单糖--葡萄糖.题中的A经氧化、还原生成的B、C、D均含有六个碳原子,可以确定A是葡萄糖,其结构简式为CH2OH(CHOH)4CHO.据题中信息可知,在发生氧化反应时,分子中的醛基(-CHO)最易被氧化为羧基(-COOH),分子式由C6H12O6变为C6H12O7,即B物质为HOCH2(CHOH)4COOH;由题目信息可知,葡萄糖A末端的-CH2OH比中间的结构较易氧化,所以-CH2OH先去氢生成醛基,再氧化为羧基,生成分子式为C6H10O8的物质,即C物质为HOOC(CHOH)4COOH;葡萄糖分子中的醛基经加氢还原生成己六醇,分子式变为C6H14O6,即D物质为HOCH2(CHOH)4CH2OH.B为一种多羟基羧酸,其结构简式为:HOCH2-CHOH-CHOH-CHOH-CHOH-COOH;(2)写出下列反应的化学方程式。
淀粉水解为葡萄糖的化学方程式: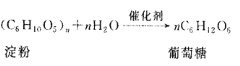 葡萄糖还原为D的化学方程式为:
葡萄糖还原为D的化学方程式为:![]() 。
。

【题目】乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂和防腐剂、乙酰苯胺的制备原理为
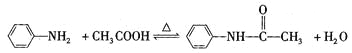
实验参数
名称 | 相对分 | 性状 | 密度(g/mL) | 沸点( | 溶解性 | |
苯胺 | 93 | 无色油状液体 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚 |
乙酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
乙酰 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,可溶于热水 | 易溶于乙醇、乙醚 |
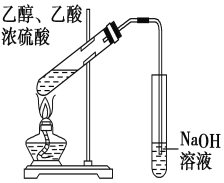
实验装置如图所示(部分仪器及夹持装置已略去)。
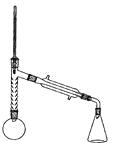
注:①刺型分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。②苯胺易被氧化。
实验步骤:
步骤1:在100mL圆底烧瓶中加入无水苯胺9.3mL、冰醋酸18.4mL、锌粉0.1g和少量沸石,安装好仪器后,对圆底烧瓶均匀加热,使反应液在微沸状态下回流,调节加热温度,使温度计温度控制在105![]() 左右;反应约60~80min,反应生成的水及少量醋酸被蒸出,当反应基本完成时,停止加热。
左右;反应约60~80min,反应生成的水及少量醋酸被蒸出,当反应基本完成时,停止加热。
步骤2:在搅拌下,趁热将蒸馏烧瓶中的液体以细流状倒入盛有冰水的100mL烧杯中,快速搅拌,乙酰苯胺结晶析出,烧杯内试剂冷却至室温后,进行抽滤、洗涤、干燥,可得到乙酰苯胺粗品。
步骤3:将乙酰苯胺粗品进行重结晶,待结晶完全后抽滤,尽量压甘干滤饼。将产品置于干净的表面皿中晾干,称重,计算产率、
请回答下列问题:
(1)实验中加入锌粉的目的是_____________________。
(2)从化学平衡的角度分析,控制温度计的温度在105![]() 左右的原因是______________。
左右的原因是______________。
(3)通过_____________可判断反应基本完成、
(4)步骤1加热可用_____________(填“水浴”或“油浴”)。
(5)洗涤乙酰苯胺粗品最合适的方法是__________________(填字母)。
A.用少量冷水洗
B.用少量热水洗
C.先用冷水洗,再用热水洗
D.用酒精洗
(6)步骤2得到的粗品中因含有某些杂质而颜色较深,步骤3重结晶的操作是:将粗品用热水溶解,加入活性炭0.1g,煮沸进行脱色,______________,再将滤液冷却结晶。
(7)该实验最终得到产品9.1g,则乙酰苯胺的产率是____________(小数点后保留两位数字。)