题目内容
11.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )| A. | 放电时负极反应为:Zn-2e-+2OH--Zn(OH)2 | |
| B. | 放电时正极发生氧化反应 | |
| C. | 放电时每转移2mol电子,反应的锌的质量是65g | |
| D. | 放电时化学能转化为电能 |
分析 根据电池反应式知,放电时,锌失电子而作负极,电极反应式为Zn-2e-+2OH-=Zn(OH)2,高铁酸钾得电子而作正极,电极反应式为FeO42-+4H2O+3e-=Fe(OH)3+5OH-,充电时,氢氧化铁失电子发生氧化反应,结合电极反应式确定电解质溶液的酸碱性.
解答 解:A.放电时,锌失电子发生氧化反应而作负极,反应为:Zn-2e-+2OH--Zn(OH)2,故A正确;
B.放电时,正极上发生还原反应,故B错误;
C.锌失电子和氢氧根离子反应生成氢氧化锌,电极反应式为Zn-2e-+2OH-=Zn(OH)2,每转移2mol电子,反应的锌的质量是65g,故C正确;
D.放电时是原电池原理,化学能转化为电能,故D正确;
故选B.
点评 本题考查化学电源新型电池,根据元素化合价变化来确定发生的反应,再结合溶液中电解质溶液浓度变化来分析解答,会根据反应物和生成物及得失电子书写电极反应式,为学习难点.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
1.下列各组中,每种物质都既有离子键又有共价键的是( )
| A. | NaOH H2SO4 (NH4)2SO4 | B. | MgO Na2SO4 HNO3 | ||
| C. | Na2O2 KOH Na3PO4 | D. | HCl Al2O3 MgCl2 |
2.痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中一种:人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上.如果将溶液①小心涂到纸上,溶液①中的溶质就跟汗渍中的物质②作用,生成物质③,物质③在光照下,分解出的银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由棕色变成黑色的指纹线.用下列化学式表示这三种物质都正确的是( )
| A. | ①AgNO3;②NaBr;③AgBr | B. | ①AgNO3;②NaCl;③AgCl | ||
| C. | ①AgCl; ②AgNO3;③NaCl | D. | ①AgNO3;②NaCl;③Ag |
19.X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g•L-1;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$.下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X>M | |
| B. | XZ2、X2M2、W2Z2均为共价化合物 | |
| C. | 由X元素形成的单质不一定是原子晶体 | |
| D. | 由Y、Z、M三种元素形成的化合物一定只有共价键 |
16.现有前20号的元素的性质或原子结构如下表:
(1)元素X的一种同位素可测定文物年代:这种同位素的符号是146C(用元素符号表示)
元素Z的离子结构示意图为 ,化合物WXY的电子式
,化合物WXY的电子式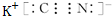 .
.
(2)元素Y与氢元素形成一种离子,则检验溶液中存在该离子的方法是:向溶液(或待测液)中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体,说明溶液中存在NH4+,反之,不存在NH4+.
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
(4)元素X与元素Y相比,非金属性较强的是N(用元素符号表示),下列表述中能证明这一事实的是bc.
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物水化物的酸性比X的最高价氧化物水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态.
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 最外层电子数比次外层电子数少5个电子 |
| W | 灼烧其化合物时通过蓝色钴玻璃片观察火焰为紫色 |
元素Z的离子结构示意图为
 ,化合物WXY的电子式
,化合物WXY的电子式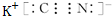 .
.(2)元素Y与氢元素形成一种离子,则检验溶液中存在该离子的方法是:向溶液(或待测液)中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体,说明溶液中存在NH4+,反之,不存在NH4+.
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
(4)元素X与元素Y相比,非金属性较强的是N(用元素符号表示),下列表述中能证明这一事实的是bc.
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物水化物的酸性比X的最高价氧化物水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态.
3.同周期的X、Y、Z三种元素,它们的气态氢化物的化学式分别为H2X、YH3、ZH4,下列说法正确的是( )
| A. | 气态氢化物的稳定性按X、Y、Z的顺序递增 | |
| B. | 三种元素的最高价氧化物对应的水化物酸性:H2ZO3>H3YO4>H2XO4 | |
| C. | 元素的最高正化合价按X、Y、Z的顺序递增 | |
| D. | 元素原子的半径按X、Y、Z的顺序递增 |
1.25℃时,将pH=2的CH3COOH溶液和pH=12的NaOH溶液等体积混合后溶液pH=a,以下关于所得溶液的关系式肯定错误的是( )
| A. | a>7 | B. | c(CH3COOH)-c(OH-)>10-amol/L | ||
| C. | c(Na+)=c(CH3COOH)+c(CH3COO-) | D. | c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |

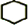 ,B名称是1,2-二溴环己烷
,B名称是1,2-二溴环己烷 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$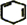 +2NaBr+2H2O.
+2NaBr+2H2O.