题目内容
13.下列实验目的无法实现的是( )| A. | 用激光笔光束鉴别氯化铁溶液和氢氧化铁胶体 | |
| B. | 用KSCN溶液鉴别Fe3+和Fe2+ | |
| C. | 用NaOH溶液和红色石蕊试纸鉴别溶液是否含NH4+ | |
| D. | 在氢氧化钠溶液中滴入氯化铁饱和溶液可以制得氢氧化铁胶体 |
分析 A.丁达尔现象为胶体特有的性质;
B.KSCN溶液鉴别Fe3+时溶液为血红色;
C.铵根离子与碱加热生成氨气,氨气可使红色石蕊试纸变蓝;
D.氢氧化钠溶液中滴入氯化铁饱和溶液,反应生成红褐色沉淀.
解答 解:A.丁达尔现象为胶体特有的性质,则用激光笔光束可鉴别氯化铁溶液和氢氧化铁胶体,故A正确;
B.KSCN溶液鉴别Fe3+时溶液为血红色,不能与亚铁离子反应,现象不同,可鉴别,故B正确;
C.铵根离子与碱加热生成氨气,氨气可使红色石蕊试纸变蓝,则试剂可鉴别铵根离子,故C正确;
D.氢氧化钠溶液中滴入氯化铁饱和溶液,反应生成红褐色沉淀,不能制备胶体,应向沸水中滴入氯化铁饱和溶液可以制得氢氧化铁胶体,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、常见离子的检验、胶体制备为解答的关键,侧重分析与实验能力的考查,注意元素化合物与实验的结合及实验评价性分析,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
11.(1)已知A、B、C、D是四种短周期元素,它们的原子序数依次增大.其中A、D元素同主族且A是原子半径最小的元素,B、C元素同周期,B的最外层电子数是次外层电子数的2倍;由A、B、C、D中的两种元素可形成原子个数比为1:1的多种化合物,甲、乙、丙为其中的三种,它们的元素组成如表所示:
常温下,甲物质为有剧毒的气体,密度略小于空气;乙物质为液体;丙物质为固体且为离子化合物.
请填写下列空白:甲的化学式为CO,乙的化学式为H2O2,丙的化学式为Na2O2,其中丙中阴离子与阳离子的个数之比为1:2.
(2)工业上常用SO2除去CO,生成物为S和CO2.
已知:S(s)+O2(g)=SO2(g)△H=a kJ/mol
CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=b kJ/mol
则反应SO2(g)+2CO(g)=S (s)+2CO (g) 的△H=(2b-a)kJ/mol
(3)为了减少CO对大气的污染,某研究性学习小组拟研究利用CO和H2O反应转化为绿色能源H2.已知:2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
则CO和H2O(g)作用生成CO2和H2的热化学方程式为CO(g)+H2O(g)=H2(g)+CO2(g)△H=-41.2KJ•moL-1
(4)某同学设计了一个CH3OH燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4的混合溶液,其装置如图:
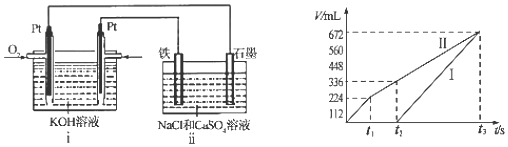
①写出ⅰ装置中通入甲醇这一极的电极反应式CH3OH+8OH--6e-=CO32-+6H2O.
②理论上ⅱ中两极所得气体的体积随时间变化的关系如坐标图所示(气体体积已换算成标准状况下的体积),则曲线I表示阴极电极上的反应情况(填“阴极”或“阳极”).写出在t1后,石墨电极上的电极反应式4OH--4e-=O2↑+2H2O (或2H2O-4e-=O2↑+4H+).
| 化合物 | 甲 | 乙 | 丙 |
| 组成元素 | B、C | A、C | C、D |
请填写下列空白:甲的化学式为CO,乙的化学式为H2O2,丙的化学式为Na2O2,其中丙中阴离子与阳离子的个数之比为1:2.
(2)工业上常用SO2除去CO,生成物为S和CO2.
已知:S(s)+O2(g)=SO2(g)△H=a kJ/mol
CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=b kJ/mol
则反应SO2(g)+2CO(g)=S (s)+2CO (g) 的△H=(2b-a)kJ/mol
(3)为了减少CO对大气的污染,某研究性学习小组拟研究利用CO和H2O反应转化为绿色能源H2.已知:2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
则CO和H2O(g)作用生成CO2和H2的热化学方程式为CO(g)+H2O(g)=H2(g)+CO2(g)△H=-41.2KJ•moL-1
(4)某同学设计了一个CH3OH燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4的混合溶液,其装置如图:

①写出ⅰ装置中通入甲醇这一极的电极反应式CH3OH+8OH--6e-=CO32-+6H2O.
②理论上ⅱ中两极所得气体的体积随时间变化的关系如坐标图所示(气体体积已换算成标准状况下的体积),则曲线I表示阴极电极上的反应情况(填“阴极”或“阳极”).写出在t1后,石墨电极上的电极反应式4OH--4e-=O2↑+2H2O (或2H2O-4e-=O2↑+4H+).
4.下列关于工业生产的叙述中,不正确的是( )
| A. | 目前工业上主要采用接触法制硫酸,并使用热交换器充分利用反应中放出的热量 | |
| B. | 从海水中提取溴,是将提取粗盐后的母液浓缩、氧化,使溶液中的溴离子发生氧化反应转化成溴单质,就得到粗溴 | |
| C. | 工业上合成氨没有采用更大的压强是从设备和动力要求方面考虑的 | |
| D. | 离子交换膜在工业生产中广泛应用,如氯碱工业使用了阳离子交换膜 |
1.“低钠盐”可以控制钠的摄入量从而防治高血压等疾病.制备“低钠盐”在食盐中用NaCl中按照配方比例添加食用KCl.国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2).
(1)测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%.该样品a的水溶液中,含量最多的离子是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种).请设计实验方案,完成下列表格.
(1)测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%.该样品a的水溶液中,含量最多的离子是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种).请设计实验方案,完成下列表格.
| 实验操作 | 预期现象及结论 |
| 步骤1:取少量样品b于烧杯中,加足量蒸馏水,并用玻璃棒搅拌 | 样品溶解,形成无色溶液. |
| 步骤2:取少量步骤1形成的溶液于试管中,再滴加少量NaOH溶液,振荡 | 有白色沉淀生成,说明样品b中添加了镁盐 |
| 步骤3:取少量步骤1形成的溶液于试管中,再滴加少量的BaCl2溶液振荡 | 若有白色沉淀产生,则添加的是MgSO4.若无明显现象,则添加的是MgCl2 |
8.短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )
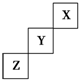

| A. | X、Y、Z三种元素中,与H2化合最容易的是X元素 | |
| B. | 最高价氧化物对应的水化物的酸性:Y>Z | |
| C. | Y的最高正化合价为+7价 | |
| D. | X单质的熔点比Z的低 |
5.下列物质中,不属于电解质的是( )
| A. | NaCl | B. | 盐酸 | C. | H2SO4 | D. | KOH |
2.下列是一些物质粒子的示意图:其中可能属于氧化物的是( )
| A. | 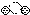 | B. | 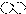 | C. |  | D. |  |
3. 短周期元素X、Y、Z、W的原子序数依次增加,其中一种为金属元素.Y元素在大气中存在两种常见单质,Z与X处于同一主族,q、r、s是由这些元素组成的二元化合物,m、n、p分别是元素Z、X、W的单质,p通常为黄绿色气体.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素X、Y、Z、W的原子序数依次增加,其中一种为金属元素.Y元素在大气中存在两种常见单质,Z与X处于同一主族,q、r、s是由这些元素组成的二元化合物,m、n、p分别是元素Z、X、W的单质,p通常为黄绿色气体.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素X、Y、Z、W的原子序数依次增加,其中一种为金属元素.Y元素在大气中存在两种常见单质,Z与X处于同一主族,q、r、s是由这些元素组成的二元化合物,m、n、p分别是元素Z、X、W的单质,p通常为黄绿色气体.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素X、Y、Z、W的原子序数依次增加,其中一种为金属元素.Y元素在大气中存在两种常见单质,Z与X处于同一主族,q、r、s是由这些元素组成的二元化合物,m、n、p分别是元素Z、X、W的单质,p通常为黄绿色气体.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 化合物Z2Y2与X2Y2中化学键完全相同 | |
| B. | 最简单氢化物的沸点:Y>W | |
| C. | 36g物质q与过量的物质r反应则有2mol电子发生转移 | |
| D. | 由Y、Z、W三种元素组成的化合物的水溶液一定显中性 |