题目内容
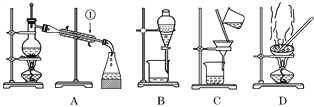
【题目】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去).
已知:2NO+CaO2═Ca(NO2)2;2NO2+CaO2═Ca(NO3)2 .
请回答下列问题:
a.向装置中通入N2 b.向三颈烧瓶中滴加稀硝酸 c.点燃酒精灯 d.熄灭酒精灯 e.停止通入氮气 f.关闭分液漏斗旋塞
(1)上述操作的正确排序为、c、、f、、 .
(2)B中盛放的试剂是 , 作用是除去(填化学式).
(3)装置E中,酸性K2Cr2O7溶液的作用:可将剩余的NO氧化成NO ![]() ,溶液由橙色变为绿色(Cr3+),反应的离子方程式是 .
,溶液由橙色变为绿色(Cr3+),反应的离子方程式是 .
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体.设计实验证明D中有亚硝酸钙生成 .
(5)整个过程持续通入氮气的作用 .
【答案】
(1)a,b,d,e
(2)蒸馏水或氢氧化钠,HNO3
(3)Cr2O72﹣+2NO+6H+=2Cr3++2NO3﹣+3H2O
(4)取少量D中反应后的固体于试管中,滴加少量稀硫酸,试管口有红棕色气体生成
(5)开始是吹出装置中的氧气,防止NO被氧化为NO2,后来是吹出装置中的NO,另外还起到防止倒吸的作用
【解析】解:(1)向装置中通入N2,吹出装置中的氧气,点燃酒精灯,向三颈烧瓶中滴加稀硝酸,铜和稀硝酸反应生成一氧化氮气体,通过装置B为氢氧化钠溶液除去气体中的硝酸,通过装置C中无水氯化钙干燥气体名通过装置D中过氧化钙反应生成Ca(NO2)2,最后通入酸性重铬酸钾可将剩余的NO氧化,操作的正确排序为:a c b f d e,
所以答案是:a、b、d、e;
(2)分析可知B中是除去一氧化氮中混有的硝酸蒸气,B中盛放的试剂是蒸馏水或氢氧化钠,作用是除去HNO3,
所以答案是:蒸馏水或氢氧化钠;HNO3;
(3)反应中Cr2O72﹣被还原成Cr3+,NO氧化成NO3﹣,离子反应方程式为:2NO+Cr2O72﹣+6H+=2Cr3++NO3﹣+3H2O;
所以答案是:2NO+Cr2O72﹣+6H+=2Cr3++NO3﹣+3H2O;
(4)Ca(NO2)2与酸会发生反应产生NO气体,NO气体遇氧气生成红棕色NO2气体,所以取少量D中反应后的固体于试管中,滴加少许硫酸,试管口有红棕色气体生成即可证明E中有亚硝酸钙生成;
所以答案是:取少量D中反应后的固体于试管中,滴加少量稀硫酸,试管口有红棕色气体生成;
(5)装置中含有空气,空气中氧气能氧化一氧化氮,所以通入氮气的目的是排除装置中氧气,防止其将生成的一氧化氮氧化生成二氧化氮,后来是吹出装置中的NO,另外还起到防止倒吸的作用,
所以答案是:开始是吹出装置中的氧气,防止NO被氧化为NO2,后来是吹出装置中的NO,另外还起到防止倒吸的作用.