题目内容
Ⅰ、已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系中共有KCl.Cl2.H2SO4.H2O.KMnO4.MnSO4.K2SO4七种物质:
(1)该反应中,化合价升高的反应物是 。
(2)写出一个包含上述七种物质的氧化还原反应方程式:
(3)上述反应中,氧化剂是 ,1 mol氧化剂在反应中得到 mol电子。
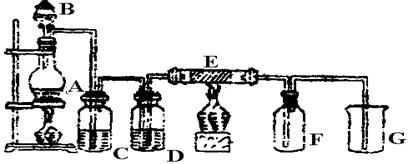
Ⅱ、某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数测定

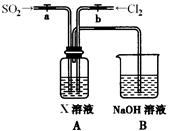
(1)装置④中的x试剂为 。
(2)装置③中发生反应的化学方程式为 。该反应是放热反应,反应温度较高时有副反应发生。改进该实验装置以减少副反应发生的方法是
_________________________。
(3)测定漂白粉有效成分的质量分数
称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.1000 mol·L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:
3ClO-+ I- = 3Cl-+ IO3- IO3- + 5I- + 3H2O = 6OH- + 3I2
实验测得数据如下表所示。
该漂白粉中有效成分的质量分数为 。若滴定过程中未充分振荡溶液局部变浅蓝色时就停止滴定,则测定结果将 (填“偏高”、“偏低”或“无影响”)
(1)该反应中,化合价升高的反应物是 。
(2)写出一个包含上述七种物质的氧化还原反应方程式:
(3)上述反应中,氧化剂是 ,1 mol氧化剂在反应中得到 mol电子。
Ⅱ、某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数测定

(1)装置④中的x试剂为 。
(2)装置③中发生反应的化学方程式为 。该反应是放热反应,反应温度较高时有副反应发生。改进该实验装置以减少副反应发生的方法是
_________________________。
(3)测定漂白粉有效成分的质量分数
称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.1000 mol·L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:
3ClO-+ I- = 3Cl-+ IO3- IO3- + 5I- + 3H2O = 6OH- + 3I2
实验测得数据如下表所示。
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
该漂白粉中有效成分的质量分数为 。若滴定过程中未充分振荡溶液局部变浅蓝色时就停止滴定,则测定结果将 (填“偏高”、“偏低”或“无影响”)
Ⅰ、(1)KCl(1分)
(2)2KMnO4+10KCl+8H2SO4=6K2SO4+2MnSO4+5Cl2+8H2O(3分)
(3)KMnO4 (1分) 5mol (2分)
Ⅱ、(1)NaOH (1分) (2)2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O(3分)
将装置③放于冷水浴中进行实验(2分) (3)42.90% (2分) 偏低(2分)
(2)2KMnO4+10KCl+8H2SO4=6K2SO4+2MnSO4+5Cl2+8H2O(3分)
(3)KMnO4 (1分) 5mol (2分)
Ⅱ、(1)NaOH (1分) (2)2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O(3分)
将装置③放于冷水浴中进行实验(2分) (3)42.90% (2分) 偏低(2分)
试题分析:Ⅰ、根据题意可知含七种物质的氧化还原反应为2KMnO4+10KCl+8H2SO4=6K2SO4+2MnSO4+5Cl2+8H2O,化合价升高的物质为KCl;氧化剂为KMnO4 ; 1mol氧化剂得电子5mol ;
Ⅱ、因为氯气有毒,所以x试剂为NaOH,吸收多余的氯气;装置③制取漂白粉,反应为2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O;为避免温度较高时发生副反应,可将装置③放于冷水浴中进行实验;(3)反应中消耗的KI的平均体积为20.00mL,其物质的量为0.1000mol/L×0.02L=0.002mol,
由题中“溶液出现稳定浅蓝色时为滴定终点”,确定应用反应(1)解题:
由关系式3ClO-~I-
3 1
n 0.002
n=0.006mol,则n(Ca(ClO)2)=0.003mol,m=0.429g,

练习册系列答案
相关题目