题目内容
饱和氯水长时间放置后,下列微粒在溶液中的物质的量增加的是
| A.Cl— | B.HClO | C.Cl2 | D.ClO— |
A
试题分析:Cl2+H2O
 HCl+HClO,HClO见光分解,导致平衡右移,且HClO
HCl+HClO,HClO见光分解,导致平衡右移,且HClO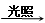 HCl,所以Cl—浓度增大。
HCl,所以Cl—浓度增大。
练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
题目内容
| A.Cl— | B.HClO | C.Cl2 | D.ClO— |
 HCl+HClO,HClO见光分解,导致平衡右移,且HClO
HCl+HClO,HClO见光分解,导致平衡右移,且HClO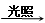 HCl,所以Cl—浓度增大。
HCl,所以Cl—浓度增大。
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案