题目内容
【题目】X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲俗称苛性钠,由X、Z、Q三种元素组成。医学中常用QR溶液配制生理盐水。化合物乙由X、R两种元素组成。请回答下列问题:

(1)Q的离子结构示意图为_________。
(2)Y元素的单质及其化合物能发生如上图所示的转化,则Y元素在元素周期表中的位置__________,在甲溶液中通入少量YZ2气体,写出该反应的离子方程式:_______________。
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。
①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为_________________________。
②下列表述中能证明Q的金属性强于W的是______(填序号)。
a.Q单质的熔点比W单质的低
b.W的原子序数大
c.Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
d.将Q、W的单质置于水中,Q单质与水剧烈反应
【答案】 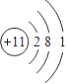 2OH-+CO2=CO32-+H2O 2Al+2OH-+2H2O═2AlO2-+3H2↑ 2Al+2OH-+2H2O═2AlO2-+3H2↑ cd
2OH-+CO2=CO32-+H2O 2Al+2OH-+2H2O═2AlO2-+3H2↑ 2Al+2OH-+2H2O═2AlO2-+3H2↑ cd
【解析】X、Y、Z、Q、W、R六种短周期元素原子序数依次增大,化合物甲俗称苛性钠,由X、Z、Q三种元素组成,X、Z、Q原子序数依次增大,所以X是H元素,Z是O元素,Q是Na元素,医学中常用QR溶液配制生理盐水,则Q为钠元素,R为氯元素,QR为氯化钠,化合物乙由H、Cl两种元素组成,所以乙是HCl;根据转化关系图可知,Y与氧气发生化合反应可生成一氧化物和二氧化物,则Y为碳元素,YZ为CO,YZ2为CO2。(1)Q是Na元素,钠原子核外有11个电子、3个电子层,钠原子结构示意为: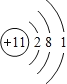 ;(2)Y为碳元素,在元素周期表中的位置为第二周期ⅣA族;在氢氧化钠溶液中通入少量二氧化碳气体,反应的离子方程式为:2OH-+CO2=CO32-+H2O;(3)W的单质既能与甲溶液反应,又能与乙溶液反应,则W为铝。①常温下,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,发生反应的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑;②a.金属单质的熔点低金属性不一定强,故错误;b.W的原子序数大,同周期金属元素原子序数越大金属性越弱,故错误;c.Na、Al两种元素金属性的强弱为Q>W,金属的金属性越强,其对应最高价氧化物的水化物碱性越强,与酸反应越容易失去电子,故正确;d.金属的金属性越强,与水或酸反应越剧烈,故将Q、W的单质置于水中,Q单质与水剧烈反应,能说明金属性Q强,故正确。答案选cd。
;(2)Y为碳元素,在元素周期表中的位置为第二周期ⅣA族;在氢氧化钠溶液中通入少量二氧化碳气体,反应的离子方程式为:2OH-+CO2=CO32-+H2O;(3)W的单质既能与甲溶液反应,又能与乙溶液反应,则W为铝。①常温下,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,发生反应的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑;②a.金属单质的熔点低金属性不一定强,故错误;b.W的原子序数大,同周期金属元素原子序数越大金属性越弱,故错误;c.Na、Al两种元素金属性的强弱为Q>W,金属的金属性越强,其对应最高价氧化物的水化物碱性越强,与酸反应越容易失去电子,故正确;d.金属的金属性越强,与水或酸反应越剧烈,故将Q、W的单质置于水中,Q单质与水剧烈反应,能说明金属性Q强,故正确。答案选cd。

 阅读快车系列答案
阅读快车系列答案