题目内容
【题目】一种利用ClO2生产NaClO2并进行尾气处理的工艺如下:
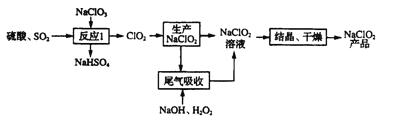
(1)写出“反应I”中生成ClO2的化学方程式:______
(2)“尾气吸收”是为了吸收未反应的ClO2,除减少污染外,还能______
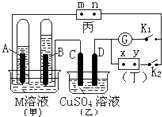
(3)实验室用右图所示装置模拟“尾气吸收”过程,发现温度较低时吸收效果好,但该反应为放热反应。在不改变吸收液浓度和体积的条件下,欲使反应在0℃~5℃下进行,实验中可采取的措施有__________
(4)为了测定获得产品中NaClO2的纯度,进行如下实验:
①准确称取1.000g上述产品,溶于水配成100.00ml,的溶液。
②取10.00mL待测液,加入过量的KI溶液,在酸性条件下发生如下反应:ClO2+4I-+4H+==2H2O+2I2+Cl-,杂质不与I-反应。
③以淀粉作指示剂,再加入0.2000mol/L Na2S2O3溶液,恰好完全反应时消耗Na2S2O3,溶液的体积为20.00mL。(已知:I2+2S2O32-=2I-+S4O62-)。计算该样品中NaClO2的纯度______。
【答案】 2NaClO3+SO2+H2SO4==2ClO2+2NaHSO4 生成NaClO2,提高NaClO2的产率或提高ClO2的利用率 给装置加冰水浴 缓慢通入ClO2 90.5%,
【解析】(1) NaClO3、SO2在酸性条件下发生氧化还原反应,生成ClO2和NaHSO4,化学方程式: 2NaClO3+SO2+H2SO4==2ClO2+2NaHSO4;正确答案:2NaClO3+SO2+H2SO4==2ClO2+2NaHSO4。
(2)从流程看出,“尾气吸收”是为了吸收未反应的ClO2,除减少污染外,还能生成NaClO2,提高NaClO2的产率或提高ClO2的利用率 ;正确答案:生成NaClO2,提高NaClO2的产率或提高ClO2的利用率。
(3)结合题给信息可知,欲使反应在0℃~5℃下进行,实验中可采取的措施有:给装置加冰水浴或缓慢通入ClO2;正确答案:给装置加冰水浴。
(4) 根据反应: I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 可知,n(I2)=
可知,n(I2)=![]() =
=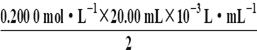 =2.000×10-3mol;n(NaClO2)=
=2.000×10-3mol;n(NaClO2)=![]() n(I2)=1.000×10-3mol;ω(NaClO2)=
n(I2)=1.000×10-3mol;ω(NaClO2)=
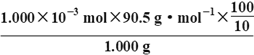 ×100%=90.50%;正确答案:90.50%。
×100%=90.50%;正确答案:90.50%。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案