题目内容
【题目】某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为![]() ,他们设计如下实验用于制取氯气并验证其性质。
,他们设计如下实验用于制取氯气并验证其性质。

请回答下列问题。
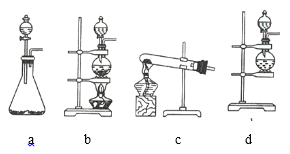
(1)该实验中A部分的装置是 _________________________________ (填序号)。
(2)B中的实验现象为 _____________________________。
(3)用离子方程式表示C中亚硫酸钠被氧化的主要原因: _____________________________。请你帮助他们设计一个实验,证明C中的亚硫酸钠已被氧化: _____________________________(简述实验步骤)。
(4)请根据题意画出D处的实验装置图,并注明装置中盛放的物质__________。
【答案】b 溶液由无色变为黄色(或棕褐色) ![]() 取少量C中的溶液,加入足量的稀盐酸,然后滴加
取少量C中的溶液,加入足量的稀盐酸,然后滴加![]() 溶液,若产生白色沉淀,则证明亚硫酸钠已被氧化
溶液,若产生白色沉淀,则证明亚硫酸钠已被氧化 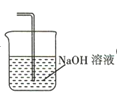 (答案合理即可)
(答案合理即可)
【解析】
根据题目信息可知漂白粉和硫酸溶液需要加热生成氯气,生成的氯气通入KI溶液,将碘离子氧化为碘单质,通入亚硫酸钠溶液中,氧化亚硫酸根,氯气有毒,过量的氯气需要进行处理。
(1)该反应的反应物是固体和液体,反应条件是加热,所以应选固液混合加热型装置b;
(2)氯气有强氧化性,通入KI溶液发生反应:2KI+Cl2=2KCl+I2,所以溶液会从由无色变为黄色(或棕褐色);
(3)氯气有强氧化性,可将亚硫酸根氧化成硫酸根,离子方程式为![]() ;亚硫酸钠被氧化生成硫酸钠,只要验证硫酸根离子的存在就可证明亚硫酸钠已经被氧化,具体方法为:取少量C中的溶液,加入足量的稀盐酸,然后滴加BaCl2溶液,若产生白色沉淀,则证明亚硫酸钠已被氧化;
;亚硫酸钠被氧化生成硫酸钠,只要验证硫酸根离子的存在就可证明亚硫酸钠已经被氧化,具体方法为:取少量C中的溶液,加入足量的稀盐酸,然后滴加BaCl2溶液,若产生白色沉淀,则证明亚硫酸钠已被氧化;
(4)氯气有毒,需要进行尾气处理,所以需要装置: 。
。

 名校课堂系列答案
名校课堂系列答案