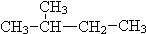题目内容
5.下列说法中正确的是( )| A. | 石油是混合物,其分馏产品汽油为纯净物 | |
| B. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| C. | 金属氧化物均为碱性氧化物 | |
| D. | “血液透析”利用了胶体的性质 |
分析 A、石油是混合物,汽油也是混合物;
B、油脂不属于高分子化合物;
C、金属氧化物不一定都是碱性氧化物,可以是两性氧化物或酸性氧化物;
D、血液是胶体,不能通过半透膜.
解答 解:A、石油是混合物,其分馏产品汽油是一定温度范围内的馏分,属于多种烃的混合物,故A错误;
B、淀粉、纤维素都属于天然高分子化合物,油脂不属于高分子化合物,故B错误;
C、金属氧化物不一定是碱性氧化物,如:Mn2O7是酸性氧化物,Al2O3是两性氧化物,故C错误;
D、血液是胶体,胶粒不能透过半透膜,故D正确;
故选D.
点评 本题考查化学基本概念,易错选项是C,注意金属氧化物不一定是碱性氧化物,为易错点,题目较简单.

练习册系列答案
相关题目
3.在生活中,需要对化学反应的速率和化学反应的限度进行研究,以便控制化学反应.
I.某实验小组以H2O2分解为例,研究浓度、催化剂、温度对反应速率的影响.按照如下方案完成实验.
通过实验得到氧气的体积与时间的关系如图1所示,回答下列问题:
(1)代表实验①的图示是Ⅳ.
(2)对比实验③和④的目的是探究催化剂对反应速率的影响.
(3)通过上面对比实验,所得的实验结论是其他条件不变,增大反应物浓度或升高温度或加入催化剂,化学反应速率加快.

Ⅱ.一定温度下,在体积为2L的恒容密闭容器中充入1molN2和3mol H2,一定条件下发生反应:
N2(g)+3H2(g)?2NH3(g),测得其中N2物质的量随时间变化如图2所示.回答下列问题:
(4)从开始反应到t2时刻,氨气的平均反应速率为$\frac{1}{2{t}_{2}}$mol/(L•min).
(5)在t3时刻,氢气的转化率为75%.
I.某实验小组以H2O2分解为例,研究浓度、催化剂、温度对反应速率的影响.按照如下方案完成实验.
| 反应物 | 催化剂 | 温度 | |
| ① | 10mL10% H2O2溶液 | 无 | 25℃ |
| ② | 10mL20% H2O2溶液 | 无 | 25℃ |
| ③ | 10mL20% H2O2溶液 | 无 | 40℃ |
| ④ | 10mL20% H2O2溶液 | 1~2滴0.1mol/LFeCl3溶液 | 40℃ |
(1)代表实验①的图示是Ⅳ.
(2)对比实验③和④的目的是探究催化剂对反应速率的影响.
(3)通过上面对比实验,所得的实验结论是其他条件不变,增大反应物浓度或升高温度或加入催化剂,化学反应速率加快.

Ⅱ.一定温度下,在体积为2L的恒容密闭容器中充入1molN2和3mol H2,一定条件下发生反应:
N2(g)+3H2(g)?2NH3(g),测得其中N2物质的量随时间变化如图2所示.回答下列问题:
(4)从开始反应到t2时刻,氨气的平均反应速率为$\frac{1}{2{t}_{2}}$mol/(L•min).
(5)在t3时刻,氢气的转化率为75%.
13. Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.
Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.
(1)若由0.2mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH>7,则混合溶液中各种离子浓度由大到小的顺序是:c(Na+)>c(A-)>c(OH-)>c(H+).
(2)若HA为弱酸,现有两组溶液
A组:由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH<7;
B组:0.1mol/L的HA溶液
①A组溶液pH<7的原因:等浓度时弱酸HA电离大于A-离子水解.
②两组溶液中c(A-)的大小,A组>B组(填“>”“<”或“=”);溶液中水的电离程度A组>B组(填“>”“<”或“=”).
(3)若HA为强酸,若是pH=2HA V1mL与pH=12Ba(OH)2 V2 mL混合后得到pH=11的溶液,则$\frac{{V}_{1}}{{V}_{2}}$=$\frac{9}{11}$
Ⅱ、现有浓度为0.1mol•L-1的五种电解质溶液①NaHSO4;②NaHCO3;③NaCl;④CH3COONa;⑤NaOH
(1)这五种溶液的pH由小到大的顺序是①<③<④<②<⑤(填编号).
(2)在上述五种溶液中分别加入Al2(SO4)3溶液,能产生大量无色无味气体的是②(填编号);其离子反应方程式为:3HCO3-+Al3+=Al(OH)3↓+3CO2↑.
Ⅲ.已知:
(1)在浓度均为0.01mol/L的CH3COONa、NaClO、Na2CO3的混合溶液中,逐滴加入0.01mol/L HCl,则体系中酸根离子反应的先后顺序为CO32-、ClO-、CH3COO-;(填酸根离子符号)
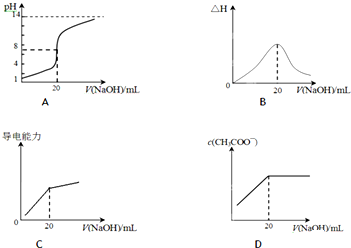
(2)25℃时,向20mL 0.1mol/L CH3COOH溶液中逐滴滴加0.1mol/L NaOH溶液,体系中各种量随着NaOH溶液的加入而变化的图象正确的是D.
 Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.
Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.(1)若由0.2mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH>7,则混合溶液中各种离子浓度由大到小的顺序是:c(Na+)>c(A-)>c(OH-)>c(H+).
(2)若HA为弱酸,现有两组溶液
A组:由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH<7;
B组:0.1mol/L的HA溶液
①A组溶液pH<7的原因:等浓度时弱酸HA电离大于A-离子水解.
②两组溶液中c(A-)的大小,A组>B组(填“>”“<”或“=”);溶液中水的电离程度A组>B组(填“>”“<”或“=”).
(3)若HA为强酸,若是pH=2HA V1mL与pH=12Ba(OH)2 V2 mL混合后得到pH=11的溶液,则$\frac{{V}_{1}}{{V}_{2}}$=$\frac{9}{11}$
Ⅱ、现有浓度为0.1mol•L-1的五种电解质溶液①NaHSO4;②NaHCO3;③NaCl;④CH3COONa;⑤NaOH
(1)这五种溶液的pH由小到大的顺序是①<③<④<②<⑤(填编号).
(2)在上述五种溶液中分别加入Al2(SO4)3溶液,能产生大量无色无味气体的是②(填编号);其离子反应方程式为:3HCO3-+Al3+=Al(OH)3↓+3CO2↑.
Ⅲ.已知:
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | HCN | 5×10-10 |
| H2CO3 | Ka1=4.2×10-7 | HClO | 3×10-8 |
| Ka2=5.6×10-11 |
(2)25℃时,向20mL 0.1mol/L CH3COOH溶液中逐滴滴加0.1mol/L NaOH溶液,体系中各种量随着NaOH溶液的加入而变化的图象正确的是D.
 )是一种镇痛和麻醉药物,可由化合物B(
)是一种镇痛和麻醉药物,可由化合物B( )通过以下路线合成得到.
)通过以下路线合成得到.
 .
. +HBr+CH3Br.
+HBr+CH3Br. 等.
等. 所示)的合成路线流程图(无机试剂任选).
所示)的合成路线流程图(无机试剂任选).
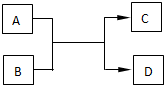 学习了元素周期表,可以帮助我们进一步丰富不同元素间的相互转化关系.已知A、B、C、D都处于短周期,A、D为单质,B、C是化合物.
学习了元素周期表,可以帮助我们进一步丰富不同元素间的相互转化关系.已知A、B、C、D都处于短周期,A、D为单质,B、C是化合物.
 ;
; 、
、 ;
; .
.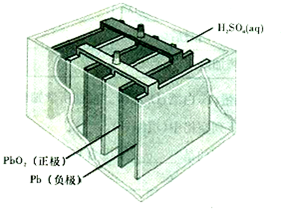
 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验: .
.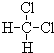 和
和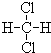 ;
;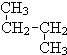 和
和 ⑦CH3 (CH2) 3CH3和
⑦CH3 (CH2) 3CH3和