题目内容
3.向混有Fe2O3的铁屑中加入足量的稀硫酸,直到固体物质完全溶解,如果得到的溶液中不含Fe3+,且产生Fe2+与H2的物质的量之比为3:1,则原混合物中Fe2O3与Fe的物质的量之比为( )| A. | 1:1 | B. | 2:5 | C. | 4:1 | D. | 3:1 |
分析 反应的反应有,Fe2O3+6H+=2Fe3++3H2O、Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+,根据产生Fe2+与H2的物质的量之比为3:1及反应的方程式列式计算.
解答 解:设原混合物中含有xmolFe,ymolFe2O3,
Fe2O3+6H+=2Fe3++3H2O
y 2y
2Fe3++Fe=3Fe2+
2y y 3y
Fe+2H+=Fe2++H2↑
(x-y) (x-y) (x-y)
则[3y+(x-y)]:(x-y)=3:1,
y:x=2:5,
即:原混合物中Fe2O3与Fe的物质的量之比为2:5,
故选B.
点评 本题考查混合物反应的计算、化学方程式的相关计算,题目难度中等,明确发生反应的实质为解答关键,注意根据方程式结合物质的性质计算.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
13.已知室温时,0.1mol•L-1 某一元酸 HA的水溶液 pH=4,则下列叙述错误的是( )
| A. | NaA 溶液呈碱性 | |
| B. | 升高温度,HA 溶液的pH 增大 | |
| C. | HA 电离平衡常数约为1×10-7 | |
| D. | 将该溶液稀释100 倍后,pH 介于4 至6 之间 |
14.下列实验能达到预期目的是( )
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸;②用NaOH溶液除去苯中的少量苯酚;③用饱和NaHCO3溶液除去CO2中的少量SO2;④用加热的方法提取NH4Cl固体中混有的少量碘;⑤用酒精萃取碘水中的碘.
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸;②用NaOH溶液除去苯中的少量苯酚;③用饱和NaHCO3溶液除去CO2中的少量SO2;④用加热的方法提取NH4Cl固体中混有的少量碘;⑤用酒精萃取碘水中的碘.
| A. | ①⑤ | B. | ①②④⑤ | C. | ②③ | D. | ②③⑤ |
11.现有1L 2mol•L-1的盐酸与100g NaOH样品配制成的溶液(杂质不与盐酸反应),则该样品中Na0H的质量分数是( )
| A. | 80% | B. | 60% | C. | 40% | D. | 20% |
18.天平两边托盘上各放等质量的烧杯,烧杯中盛放等体积、等浓度的稀硫酸,若向两个烧杯中分别放人一块锌片和一块铁片,充分反应后,金属均有剩余且天平仍保持平衡,则最初锌和铁的物质的量之比为( )
| A. | 1:1 | B. | 54:63 | C. | 56:65 | D. | 65:56 |
8.下列有关混合物分离方法和原理分析都正确的是( )
| 选项 | 操作方法 | 实验原理 |
| A | 铁粉中混有少量铝粉:溶于浓氢氧化钠溶液,过滤 | 铝粉与氢氧化钠溶液反应,铁粉不和氢氧化钠溶液反应 |
| B | 氯化亚铁溶液中混有氯化铁:加入足量铜粉,过滤 | 铜能将Fe3+还原成Fe2+,铜与Fe2+不反应 |
| C | 过氧化钠中混有氧化钠:在空气中灼烧固体 | 氧化钠与氧气在加热条件下生成过氧化钠 |
| D | 氯化铝溶液中混有氯化镁:加入足量氢氧化铝,过滤 | 氯化镁水解生成盐酸,盐酸与氢氧化铝反应,促进Mg2+完全水解 |
| A. | A | B. | B | C. | C | D. | D |
15.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 0.1mol•L-1 CH3COONa溶液与0.1mol•L-1 CH3COOH溶液等体积混合(pH=4.75):c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| C. | 0.1mol•L-1 CH3COONa溶液与0.1mol•L-1 HCl溶液混合至pH=7:c(Na+)>c(Cl-)=c(CH3COOH)>c(CH3COO-) | |
| D. | 0.1mol•L-1 Na2CO3溶液与0.1mol•L-1 NaHCO3溶液等体积混合:c(HCO3)+2c(H+)+3c(H2CO3)=c(CO32-)+2c(OH-) |
11.如图实验方案能达到实验目的是( )
| A. | 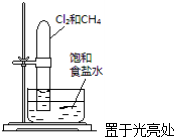 验证甲烷与氯气发生化学反应 | B. | 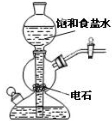 实验室制乙炔 | ||
| C. |  从碘与氯化钠的混合溶液中分离碘 | D. | 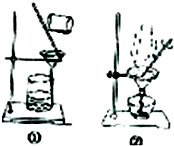 粗苯甲酸的提纯 |