题目内容
17.用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )| A. | 1 mol的氢氧根离子所含电子数均为9 NA | |
| B. | 1.00 mol NaCl中含有NA个NaCl分子 | |
| C. | 常温常压下,92g的NO2和N2O4的混合气体含有的原子数为6NA | |
| D. | 常温常压下,22.4L氯气与足量铁粉充分反应,转移的电子数为2NA |
分析 A、OH-为10电子微粒;
B、NaCl是离子晶体,不含分子;
C、NO2和N2O4的最简式均为NO2;
D、常温常压下,气体摩尔体积大于22.4L/mol.
解答 解:A、OH-为10电子微粒,故1mol氢氧根含10mol电子,即10NA个,故A错误;
B、NaCl是离子晶体,不含分子,1.00 mol NaCl中含有NA个Na+和NA个Cl-,故B错误;
C、NO2和N2O4的最简式均为NO2,故92g混合气体中的NO2的物质的量n=$\frac{92g}{46g/mol}$=2mol,则含6mol原子,即6NA个,故C正确;
D、常温常压下,气体摩尔体积大于22.4L/mol,故UAN22.4L氯气的物质的量小于1mol,则与足量的铁反应转移的电子的物质的量小于2mol,即小于2NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
8.物质的量浓度都是0.1mol/L的CH3COOH和CH3COONa混合溶液,已知其中c(CH3COO-)>c(Na+),对该溶液的下列判断正确的是( )
| A. | c(H+)<c(OH-) | B. | c(CH3COOH)+c(CH3COO-)=0.2mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(CH3COO-)+c(OH-)=0.1mol/L |
5.下列叙述正确的是( )
| A. | 除去乙烷中少量的乙烯:通过KMnO4溶液,再用浓硫酸干燥 | |
| B. | 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液 | |
| C. | 鉴别溴乙烷中的溴原子,可直接加入AgNO3溶液 | |
| D. | 除去乙醇中少量的水:加足量生石灰,蒸馏 |
12.辛烷的分子式是( )
| A. | C6H14 | B. | C7H16 | C. | C8H18 | D. | C8H16 |
2.有一种有机物结构简式为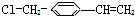 推测它不可能具有下列哪种性质( )
推测它不可能具有下列哪种性质( )
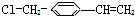 推测它不可能具有下列哪种性质( )
推测它不可能具有下列哪种性质( )| A. | 能被酸性高锰酸钾溶液氧化 | B. | 能使溴水发生加成反应而褪色 | ||
| C. | 能发生水解反应 | D. | 易溶于水,也易溶于有机溶剂 |
9.关于化学键的各种叙述中,下列说法中正确的是( )
| A. | 含有金属元素的化合物一定是离子化合物 | |
| B. | 共价化合物里,一定不存在离子键 | |
| C. | 由多种非金属元素组成的化合物一定是共价化合物 | |
| D. | 由不同种元素组成的多原子分子里,一定只存在极性键 |
6.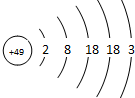 张青莲是我国著名的化学家.1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中的首次采用我国测定的原子量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
张青莲是我国著名的化学家.1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中的首次采用我国测定的原子量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
 张青莲是我国著名的化学家.1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中的首次采用我国测定的原子量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
张青莲是我国著名的化学家.1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中的首次采用我国测定的原子量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )| A. | In在反应中容易失电子 | |
| B. | In为长周期元素 | |
| C. | In的最高价氧化物对应的水化物为强碱 | |
| D. | In为过渡元素 |
9.关于如图所示的氢氧燃料电池的说法错误的是( )
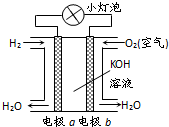

| A. | 电极a是负极 | |
| B. | 电极b上的电极反应为O2+2H2O+4e-=4OH- | |
| C. | 外电路中电子由电极b流向电极a | |
| D. | 氢氧燃料电池的优点是高效、对环境友好 |