题目内容
7.已知氨水的密度随浓度的减小而增大,现将50g浓度为cmol•L-1,密度为ρg•cm-3的氨水中加入一定量的水稀释成0.5cmol•L-1,则加入水的体积为( )| A. | 小于50mL | B. | 等于50mL | C. | 大于50mL | D. | 等于50/ρmL |
分析 计算出50g浓度为cmol•L-1、密度为ρ g•cm-3的氨水的体积,令稀释后氨水的体积为Vml,根据稀释定律,稀释前后溶质的物质的量不变,据此列式计算V的值.令稀释后的密度为xg/ml,氨水浓度越小,密度越大,则x>ρ,计算稀释后氨水的质量,稀释后氨水的质量减去50g即为需加水的质量,根据v=$\frac{m}{ρ}$计算水的体积.根据稀释前后氨水密度判断水的体积.
解答 解:50g浓度为cmol•L-1、密度为ρ g•cm-3的氨水的体积为$\frac{50g}{ρg/mL}$=$\frac{50}{ρ}$mL,
令稀释后氨水的体积为Vml,根据稀释定律,稀释前后溶质的物质的量不变,则:$\frac{50}{ρ}$mL×cmol/L=VmL×0.5cmol/L
解得V=$\frac{100}{ρ}$mL,
令稀释后的密度为xg/ml,氨水浓度越小,密度越大,则x>ρ,
稀释后氨水的质量为$\frac{100}{ρ}$mL×xg/ml=$\frac{100x}{ρ}$g,
所以加入的水的质量为$\frac{100x}{ρ}$g-50g=($\frac{100x}{ρ}$-50)g,
所以加入的水的体积为$\frac{(\frac{100x}{ρ}-50)g}{1g/mL}$=($\frac{100x}{ρ}$-50)mL
由于x>ρ,所以($\frac{100x}{ρ}$-50)>50ml,
故选C.
点评 本题考查物质的量浓度有关计算,为高频考点,侧重考查学生分析计算能力,明确物质的量浓度大小与密度大小关系是解本题关键,题目难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
15.某化学反应的能量变化如图所示.下列有关叙述正确的是( )
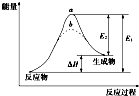

| A. | 逆反应的活化能小于正反应的活化能 | |
| B. | a、b分别对应有催化剂和无催化剂的能量变化 | |
| C. | 该反应的反应热△H=E2-E1 | |
| D. | 催化剂能改变反应的焓变 |
12.设 NA代表阿伏加德罗常数,下列说法中正确的是( )
| A. | 标准状况下,22.4L CO完全燃烧生成CO2分子数为NA | |
| B. | 17g 氨气所含电子数为NA | |
| C. | 在常温、常压下,11.2L氯气所含的原子数目为NA | |
| D. | 32g氧气所含的原子数目为NA |
19.铜镁合金1.52g完全溶解于50mL密度为1.40g•mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况).向反应后的溶液中加入1.0mol•L-1 NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol•L-1 | |
| C. | 该合金中铜与镁的物质的量之比是2:1 | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
16.相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:A (g)+3B (g)?2C (g)△H=-50kJ/mol
实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是( )
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| A | B | C | ||
| (1) | 1 | 3 | 0 | 放出热量a kJ |
| (2) | 0 | 0 | 2 | 吸收热量b kJ |
| (3) | 2 | 6 | 0 | 放出热量c kJ |
| A. | A的体积分数:(2)>(1)>(3) | |
| B. | 三个容器内反应的平衡常数:K(3)=K2(1)=K2(2) | |
| C. | 达平衡时体系压强:P(3)=2P(1) | |
| D. | 热量关系:a+b=50 |
17.向盛有100mL 0.5mol•L-1的硫酸溶液中加入25mL 0.8mol•L-1的氯化钡溶液,过滤后,向滤液中滴加氢氧化钠溶液中和其酸性,需2.5mol•L-1的氢氧化钠溶液( )
| A. | 100mL | B. | 40mL | C. | 25mL | D. | 20mL |