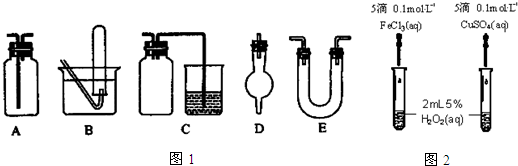
题目内容
11.饮料果醋中含有苹果酸(MLA),其分子式为C4H6O5.0.1mol苹果酸与足量NaHCO3溶液反应能产生4.48L CO2(标准状况),苹果酸脱水能生成使溴水褪色的产物.苹果酸经聚合生成聚苹果酸(PMLA).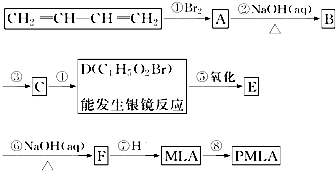
(1)B的结构简式为:HOCH2CH=CHCH2OH,D中官能团的名称是醛基、溴原子.
(2)MLA的核磁共振氢谱有5组峰.任写一种与MLA具有相同官能团的同分异构体的结构简式HOOCC(OH)(CH3)COOH 或HOOCCH(CH2OH)COOH.
(3)写出E→F转化的化学方程式:HOOCCH2CHBrCOOH+3NaOH$\stackrel{△}{→}$NaOOCCH2CH(OH)COONa+NaBr+2H2O,
(4)上述转化关系中步骤③和④的顺序能否颠倒?不能(填“能”或“不能”),说明理由:若先氧化则B中碳碳双键也被氧化
(5)写出聚苹果酸(PMLA)的一种可能的结构简式
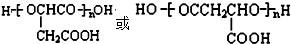 .
.
分析 苹果酸(MLA)分子式为C4H6O5,0.l mol苹果酸与足量NaHCO3溶液反应能产生4.48L CO2(标准状况),二氧化碳的物质的量为0.2mol,则1mol苹果酸含2mol-COOH.苹果酸脱水能生成使溴水褪色的产物,应含有1个-OH,结合苹果酸的分子式知,苹果酸的结构简式为:HOOCCH2CH(OH)COOH.苹果酸酯化反应进行的聚合生成聚苹果酸(PMLA),其结构为 .
.
D被氧化生成E,则E中含有溴原子,E和氢氧化钠的水溶液发生反应生成F,F酸化生成MLA,所以F的结构简式为:NaOOCCH2CH(OH)COONa,E的结构简式为:HOOCCH2CHBrCOOH,D能发生银镜反应则D中含有醛基,所以D的结构简式为:OHCCH2CHBrCHO,根据1,3-丁二烯及D的结构简式知,1,3-丁二烯和溴发生1,4-加成生成A为BrCH2CH=CHCH2Br,A和氢氧化钠的水溶液发生取代反应生成B为HOCH2CH=CHCH2OH,B与HBr发生加成反应生成C,C的结构简式为:HOCH2CH2CHBrCH2OH,C再被氧化生成D,苹果酸经聚合生成聚苹果酸(PMLA),据此解答.
解答 解:苹果酸(MLA)分子式为C4H6O5,0.l mol苹果酸与足量NaHCO3溶液反应能产生4.48L CO2(标准状况),二氧化碳的物质的量为0.2mol,则1mol苹果酸含2mol-COOH.苹果酸脱水能生成使溴水褪色的产物,应含有1个-OH,结合苹果酸的分子式知,苹果酸的结构简式为:HOOCCH2CH(OH)COOH.苹果酸酯化反应进行的聚合生成聚苹果酸(PMLA),其结构为 .
.
D被氧化生成E,则E中含有溴原子,E和氢氧化钠的水溶液发生反应生成F,F酸化生成MLA,所以F的结构简式为:NaOOCCH2CH(OH)COONa,E的结构简式为:HOOCCH2CHBrCOOH,D能发生银镜反应则D中含有醛基,所以D的结构简式为:OHCCH2CHBrCHO,根据1,3-丁二烯及D的结构简式知,1,3-丁二烯和溴发生1,4-加成生成A为BrCH2CH=CHCH2Br,A和氢氧化钠的水溶液发生取代反应生成B为HOCH2CH=CHCH2OH,B与HBr发生加成反应生成C,C的结构简式为:HOCH2CH2CHBrCH2OH,C再被氧化生成D,苹果酸经聚合生成聚苹果酸(PMLA).
(1)由上述分析可知,B为HOCH2CH=CHCH2OH,D为OHCCH2CHBrCHO,含有官能团有:醛基、溴原子,
故答案为:HOCH2CH=CHCH2OH;醛基、溴原子;
(2)MLA为HOOCCH2CH(OH)COOH,核磁共振氢谱有5组峰,任意一种与MLA具有相同官能团的同分异构体的结构简式为:HOOCC(OH)(CH3)COOH 或HOOCCH(CH2OH)COOH,
故答案为:5;HOOCC(OH)(CH3)COOH 或HOOCCH(CH2OH)COOH;
(3)E→F转化的化学方程式为:HOOCCH2CHBrCOOH+3NaOH$\stackrel{△}{→}$NaOOCCH2CH(OH)COONa+NaBr+2H2O,
故答案为:HOOCCH2CHBrCOOH+3NaOH$\stackrel{△}{→}$NaOOCCH2CH(OH)COONa+NaBr+2H2O;
(4)顺序不能颠倒,若先氧化则B中碳碳双键也被氧化,
故答案为:不能,若先氧化则B中碳碳双键也被氧化;
(5)苹果酸经聚合生成聚苹果酸(PMLA),PMLA的可能结构简式为: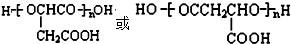 ,
,
故答案为: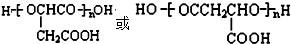 .
.
点评 本题考查有机物的推断,明确苹果酸的性质来推断其结构是解答本题的关键,熟悉醇、羧酸、烯烃的性质即可解答,题目难度中等.

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
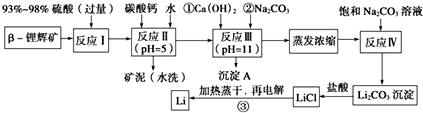
(1)用氧化物形式表示LiAlSi2O6的组成:Li2O•Al2O3•4SiO2.
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4;控制pH,使Fe3+、Al3+完全沉淀.
(3)写出反应Ⅲ中生成沉淀A的离子方程式:Mg2++2OH-═Mg(OH)2↓、Ca2++CO32-═CaCO3↓.
(4)洗涤所得Li2CO3沉淀要使用热水(选填“热水”或“冷水”),你选择的理由是Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗.
(5)将氯化锂溶液蒸干的过程中还需不断通入HCl气体,其作用是抑制LiCl的水解,防止生成LiOH,同时HCl可带走水蒸气
(6)本实验在电解熔融氯化锂生产锂时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
①已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的燃烧热为△H=-241.8kJ•mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)═Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
| 共价键 | C-C | C═C | C-H | H-H |
| 键能/(kJ•mol-1) | 348 | 610 | 413 | 436 |
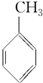 (g)+3H2(g)→
(g)+3H2(g)→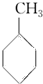 (g)的反应热;
(g)的反应热;⑤由盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等;
⑥25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热.
| A. | ①②③④ | B. | ③④⑤ | C. | ④⑤ | D. | ⑥ |
| A. | 氯化铵和过氧化氢的分解 | B. | 二氧化硅与二氧化碳的熔化 | ||
| C. | 蔗糖和干冰的熔化 | D. | 氯化镁和氯化铝的熔化 |
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的变化的曲线是b,用O2表示从0=2s内该反应的平均速率v(O2)=0.0015mol/(L•s).
(3)能说明该反应一定达到平衡状态的是bd

a.v(NO2)=2v(O2)
b.容器内颜色保持不变
c.2V逆 (NO)=v正(O2)
d.容器内压强保持不变
(4)能增大该反应的反应速率是bcd
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂.
| A. | 称取25g胆矾溶解在1L水中 | |
| B. | 将16g胆矾溶于水,然后将此溶液稀释至1L | |
| C. | 称取25g胆矾溶于水,然后将此溶液稀释至1L | |
| D. | 将胆矾加热除去结晶水后,称取16g溶解在1L水中 |
| A. | 取代 加成 水解 | B. | 消去 加成 水解 | C. | 水解 消去 加成 | D. | 消去 水解 取代 |