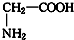题目内容
16.(1)在硫酸铜晶体里结晶水含量的测定实验中,称量操作至少要进行4次.(2)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、环形玻璃搅拌棒、量筒.
(3)图1是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体).

请回答下列问题:
①能用作干燥氨气的装置有DE(填字母);
②既能用于收集氯气又能用于收集一氧化氮气体的装置有AB(填字母);
③在实验室制备氯气的实验中,用以除去氯气中氯化氢等杂质气体的装置有A (填字母);
④能用于乙烯与溴水反应制二溴乙烷的实验装置有A(填字母);
⑤在C装置中,若用烧杯内的氢氧化钠溶液吸收尾气二氧化硫,则广口瓶的作用是防止倒吸.
(4)为比较Fe3+和Cu2+对H2O2分解的催化效果,某同学设计了图2所示的实验.
①可通过观察以生成的气体O2快慢来判断反应的快慢来定性的得出结论;
②有A同学提出将CuSO4改为CuCl2更为合理,其理由是使阴离子相同,排除阴离子的干扰;若不采用A同学的改进方案,你认为还可以如何改进?将FeCl3改为Fe2(SO4)3.
分析 (1)在加热时,为了保证结晶水全部失去,称量操作至少要进行4次;
(2)依据中和热测定需要的仪器回答即可;
(3)①氨气为碱性气体,常用碱性干燥剂碱石灰固体干燥,以此选择所用仪器;
②一氧化氮易与氧气反应,只能用排水法收集;
③除去氯气中氯化氢等杂质气体的装置应为洗气瓶,只有A可以;
④乙烯与溴水反应制二溴乙烷的实验为气体和液体的反应,所用仪器具有双孔橡皮塞;
⑤易溶的气体收集需要防止倒吸;
(4)①比较反应速率的大小可通过生成气体的快慢来判断;
②比较不同催化剂的催化效果,应排除其它因素的干扰.
解答 解:(1)实验中的加热、冷却、称量的操作步骤要重复进行,直至连续两次称量的差不超过0.1 g为止,一般情况下,结晶水含量测定时称量次数不得少于四次,故答案为:4;
(2)中和热的测定实验中需要用的主要玻璃仪器有:二只大小不同的烧杯、二只大小相同的量筒、温度计、环形玻璃搅拌捧,
故答案为:环形玻璃搅拌棒、量筒;
(3)①氨气为碱性气体,常用碱性干燥剂碱石灰固体干燥,而碱石灰只能填装在D、E中,故答案为:D、E;
②氯气既可用向上排空气法收集可用A,也可用排饱和食盐水收集用B,一氧化氮易与氧气反应2NO+O2=2NO2,一氧化氮密度与空气密度相当,所以只能用排水法收集,所以既能用于收集氯气又能用于收集一氧化氮气体的装置只能用B,故答案为:B;
③除去氯气中氯化氢等杂质气体的装置应为洗气瓶,A用作洗气瓶,装有饱和食盐水,长管进短管出,故答案为:A;
④乙烯与溴水反应CH2=CH2+Br2→CH2BrCH2Br,A装置具有双孔橡皮塞,可用作乙烯与溴水反应制二溴乙烷的实验装置,乙烯从长导管进入,瓶中装有溴水,故答案为:A;
⑤二氧化碳易溶于氢氧化钠中,安全瓶的作用是防止倒吸,故答案为:防止倒吸;
(4)①比较反应速率的大小可通过生成气体的快慢来判断,根据2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑可知,以生成的气体O2快慢来判断反应的快慢,故答案为:以生成的气体O2快慢来判断反应的快慢;
②比较不同催化剂的催化效果,应排除其它因素的干扰,氯化铁和硫酸铜中阴阳离子都不同,无法判断是阴离子起作用还是阳离子起作用;将CuSO4改为CuCl2或将FeCl3改为Fe2(SO4)3阴离子相同,可以消除阴离子不同对实验的干扰,故答案为:由于CuSO4、FeCl3中的阴离子不同,不能排除阴离子的因素;将FeCl3改为Fe2(SO4)3.
点评 本题考查了硫酸铜结晶水的检验、实验室中常见气体的收集与除杂、催化剂的作用及化学反应速率的影响因素等知识点,题目有一定的难度.

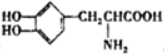 ,下列关于它的叙述正确的是( )
,下列关于它的叙述正确的是( )| A. | L-多巴只含有2中官能团 | |
| B. | L-多巴不能发生肽反应 | |
| C. | L-多巴既具有酸性,又具有碱性 | |
| D. | 1molL-多巴只能与含1molNaOH的溶液反应 |
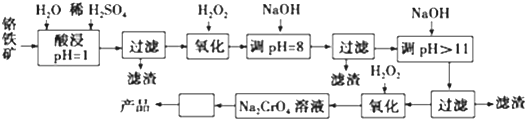
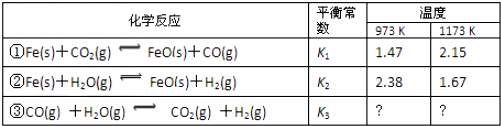
已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO2-形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下.
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | 9.0 | -- | -- |
| 沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8 | 9(>9溶解) |
(2)流程图中“□”内的操作是蒸发浓缩、冷却结晶.
(3)加入NaOH调节溶液的pH=8时,被除去的离子是Fe3+、Al3+;调节溶液的pH>11时,被除去的离子是Mg2+.
(4)“调pH=8”和“调pH>11”中间的“过滤”步骤能否省略,为什么?不能,当pH=8时Al3+已经完全转化为Al(OH)3,若不经过滤除去,当继续加入NaOH时Al(OH)3会溶解,引入杂质离子AlO2-.
| A. | 1molFeI2与足量氯气反应时转移的电子数为3NA | |
| B. | 1L2mol•L-1 K2S溶液中S2-和HS-的总数为2NA | |
| C. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| D. | 50mL18mol•L-1浓硫酸与足量铜微热反应,转移的电子数为1.8NA |
①甘氨酸 ②丙氨酸 ③苯丙氨酸 ④谷氨酸
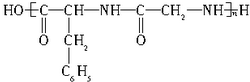
| A. | ①② | B. | ③④ | C. | ②③ | D. | ①③ |
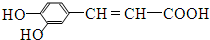 .下列有关咖啡酸的说法中,不正确的是( )
.下列有关咖啡酸的说法中,不正确的是( )| A. | 咖啡酸分子中的所有原子不可能共平面 | |
| B. | 咖啡酸可以发生还原、酯化、加聚、显色等反应 | |
| C. | 1mol咖啡酸可与4 mol Br2发生反应 | |
| D. | 1mol咖啡酸与NaOH溶液反应最多消耗1mol的NaOH |
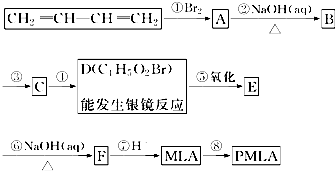
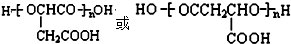 .
.
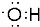 ,(CH3)3COH的名称2-甲基-2-丙醇(系统命名法)
,(CH3)3COH的名称2-甲基-2-丙醇(系统命名法)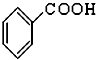 ⑤CH3CHO ⑥
⑤CH3CHO ⑥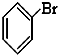
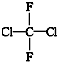 和
和 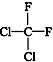 ⑥
⑥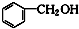 和
和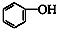 ⑦CH3CH2NO2和
⑦CH3CH2NO2和