题目内容
【题目】砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途回答下列问题:
(1)写出砷的原子序数______________
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H2AsO4和单质硫,写出发生反应的化学方程式 _____________________________________________;该反应需要在加压下进行,原因是 _______________________________________
(3)已知:As(s)+3/2H2(g)+2O2(g)=H3AsO4 (s) △H1
H2(g)+1/2O2(g)=H2O(l) △H2
2As(s)+5/2O2(g)=As2O5(s) △H3
则反应As2O5(s)+3H2O(l)=2H3AsO4 (s)的△H= ________________________
(4)298K时,将20mL 3xmol·L-1Na3AsO3、20mL 3xmol·L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-![]() AsO43-(aq)+2I-(aq)+H2O(l)溶液中c(AsO43-)与反应时间(t)的关系如图所示.
AsO43-(aq)+2I-(aq)+H2O(l)溶液中c(AsO43-)与反应时间(t)的关系如图所示.
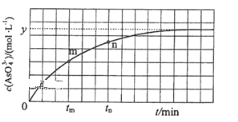
①下列可判断反应达到平衡的是 ______ (填标号).
a.溶液的pH不再变化 b.v(I-)=2v(AsO33-)
c.c(AsO43-)/c(AsO33-)不再变化 d.c(I-)=ymol·L-1
②tm时,v正______v逆 ( 填“大于”“小于”或“等于”)
③tm时,v逆 ______tn时v逆(填“大于”“小于”或“等于”),理由是 ____________________
④若平衡时溶液pH=14,则该反应的平衡常数K为 ______________
【答案】33 2As2O3+5O2+6H2O=4H3AsO4+6S 加压反应速率增大,而且平衡右移,可提高生产效率 2△H1-3△H2-△H3 ac 大于 小于 tm时生成物AsO43-的浓度更小,故逆反应速率更慢 4y3/(x-y)2
【解析】
(1)砷元素原子序数为33,原子核外有四个电子层,最外层5个电子,原子结构示意图为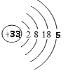 ,故答案为:
,故答案为: ;
;
(2)工业上常将含砷废渣(主要成分为As2O3)制成浆状,通入O2氧化,生成H3AsO4和单质硫,砷元素化合价+3价变化为+5价,反应的化学方程式为2As2S3+5O2+6H2O=
4H3AsO4+6S,增大压强,可增大反应速率,并使平衡正向移动,增大反应物的转化率,故答案为:2As2S3+5O2+6H2O=4H3AsO4+6S;加压反应速率增大,而且平衡右移,可提高生产效率;
(3)已知:①As(s)+ 3/2H2(g)+2O2(g)=H3AsO4(s)△H1②H2(g)+1/2O2(g)=H2O(l)△H2③2As(s)+5/2O2(g)=As2O5(s)△H3,则利用盖斯定律将①×2-②×3-③可得As2O5(s)+3H2O(l)=2H3AsO4(s)△H=2△H1-3△H2-△H3,故答案为:2△H1-3△H2-△H3;
(4)①a.溶液pH不变时,则c(OH-)也保持不变,反应达到平衡状态,故a正确;
b.同一个化学反应,速率之比等于化学计量数之比,无论是否达到平衡,都存在v(I-)=2v(AsO33-),故b错误;
c.c(AsO43-)/c(AsO33-)不再变化,可说明各物质的浓度不再变化,反应达到平衡状态,故c正确;
d.由图可知,当c(AsO43-)=ymolL-1时,浓度不再发生变化,则达到平衡状态,由方程式可知此时c(I-)=2ymolL-1,所以c(I-)=ymolL-1时没有达到平衡状态,故d错误,故答案为:ac;
②反应从正反应开始进行,tm时反应继续正向进行,则v正大于v逆,故答案为:大于;
③tm时比tn时浓度更小,则逆反应速率更小,故答案为:小于;tm时AsO43-浓度更小,反应速率更慢;
④反应前,三种溶液混合后,Na3AsO3的浓度为3xmol/L×20/(20+20+20)=xmol/L,同理I2的浓度为xmol/L,反应达到平衡时,生产c(AsO43-)为ymol/L,则反应生产的c(I-)=2ymol/L,消耗的AsO33-、I2的浓度均为ymol/L,平衡时c(AsO33-)=(x-y)mol/L,c(I2)=(x-y)mol/L,溶液中c(OH-)=1mol/L,则K=y(2y)2/(x-y)(x-y)×12=4y3/(x-y)2,故答案为:4y3/(x-y)2。