题目内容
【题目】电动公交车替代燃油公交车是节能减排、控制雾霾的重要举措之一,下图所示电池是一种正在开发的车载电池。有关该电池的说法正确的是
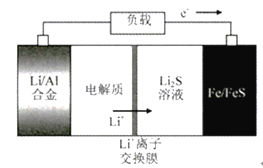
A. 放电时Fe/FeS极是负极
B. 放电时负极反应式为:Al-3e-=Al3+
C. 充电时阳极反应式为:Fe+S2--2e-=FeS
D. 左边电解质可以是LiOH的醇溶液
【答案】C
【解析】放电时为原电池,根据图示电子流向可知,电子由负极流向正极,因此Fe/FeS极是正极,A错误;放电时,Fe/FeS极是正极,锂/铝合金为负极,发生氧化反应,锂比铝活泼,所以:Li-e-=Li+B错误;充电时,为电解池,阳极发生氧化反应,铁失电子变为亚铁离子,Fe+S2--2e-=FeS,C正确;LiOH在醇溶液中不能发生电离产生锂离子,没有自由移动的离子,不能构成闭合回路,D错误;正确选项C。

练习册系列答案
相关题目
【题目】下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
水的离子积常数 | 1×10﹣14 | α | 1×10﹣12 |
试回答下列问题:
(1)若25<t1<t2 , 则α1×10﹣14(填“>”“<”或“=”),作出此判断的理由是 .
(2)25℃下,某Na2SO4溶液中c(SO42﹣)=5×10﹣4 molL﹣1 , 取该溶液1mL,加水稀释至10mL,则稀释后溶液中c (Na+):c (OH﹣)= .
(3)t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2= . 此溶液中各种离子的浓度由大到小的排列顺序是 .