题目内容
2.“5•12”地震给四川等省市人民群众带来巨大的灾难.在灾区经常发生因混合使用消毒剂或洁污剂而产生的氯气中毒事件,据此推测,产生类似中毒事件的相混合的洁污剂或消毒剂中最有可能含有的离子或物质是( )| A. | ClO3-,Cl-,K+ | B. | ClO-,Cl-,H+ | ||
| C. | NaClO,NaClO3,NaNO3 | D. | NaClO,Na2SO4,NaCl |
分析 由信息可知因混合使用消毒剂或洁污剂而产生的氯气中毒事件,则发生ClO-+Cl-+2H+=H2O+Cl2↑,以此来解答.
解答 解:A、C、D中的物质之间不能反应,不会生成氯气,只有B中发生ClO-+Cl-+2H+=H2O+Cl2↑,即只有B符合题意,
故选B.
点评 本题考查离子共存及离子反应,为高频考点,把握发生的氧化还原反应及消毒剂、洁污剂中的成分为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
12.下列物质在一定条件下能被氧化生成醛的是( )
| A. |  | B. | 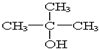 | C. |  | D. |  |
13.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液.不正确的操作顺序是( )
| A. | ⑤②④①③ | B. | ⑤④②①③ | C. | ②⑤④①③ | D. | ①④②⑤③ |
10.下列各组物质,不用任何试剂即可鉴别的是( )
| A. | NaCl、NaBr、KI三种无色溶液 | |
| B. | HCl、CaCl2、NaNO3、Na2CO3四种溶液 | |
| C. | NaBr、HCl、KCl三种溶液 | |
| D. | 氯化钠、淀粉碘化钾、溴化钾、溴水四种溶液 |
17. 在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得
在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得
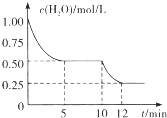
c( H2O)随反应时间(t)的变化如图所示.下列判断正确的是( )
 在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得
在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得c( H2O)随反应时间(t)的变化如图所示.下列判断正确的是( )
| A. | 0-5 min内,v(H2)=0.05 mol/(L.min) | |
| B. | 5 min时该反应的K值一定小于12 min时的K值 | |
| C. | 10 min时,改变的外界条件可能是减小压强 | |
| D. | 5 min时该反应的v正大于11 min时的v逆 |
7.下列反应的离子方程式书写正确的是( )
| A. | 向饱和Ca(HCO3)2溶液中加入足量的NaOH溶液:Ca2++HCO${\;}_{3}^{-}$+OH-═CaCO3↓+H2O | |
| B. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | |
| C. | 1L2mol•L-1的FeBr2溶液中通入2.5mol Cl2:4Fe2++6Br-+5Cl2═10Cl-+4Fe3++3Br2 | |
| D. | 以石墨作电极电解CuCl2溶液:2Cl-+2H2O═2OH-+Cl2↑十H2↑ |
14.下列说法或叙述不正确的是( )
| A. | 蛋白质“溶液”是一种胶体,向该分散系中加入少量的盐(如硫酸铵)能促进蛋白质的溶解 | |
| B. | 饱和(NH4)2SO4溶液能使蛋白质变性 | |
| C. | 用半透膜可除去蛋白质溶液中的NaCl | |
| D. | 用灼烧的方法检验是毛线还是棉线 |
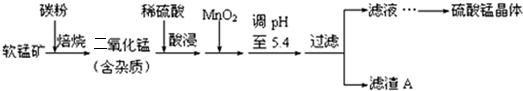
4.工业上利用软锰矿(主要成分为MnO2,同时含少量铁、铝等的化合物)制备硫酸锰的常见流程如下:
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
(1)一氧化锰用硫酸酸浸时发生的主要反应的离子方程式为MnO+2H+=Mn2++H2O.酸浸后加入MnO2将溶液中的Fe2+氧化成Fe3+,其目的是确保铁元素在后续操作中完全转化为氢氧化物沉淀而除去.
(2)滤渣A的成分除MnO2外,还有Fe(OH)3和Al(OH)3.
(3)MnO2是制造碱性锌锰电池的基本原料,放电时负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2.工业上以石墨为电极电解酸化的MnSO4溶液生产MnO2,阳极的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+,当阴极产生4.48L(标况)气体时,MnO2的理论产量为17.4g.
(4)锰的三种难溶化合物的溶度积:Ksp(MnCO3)=1.8×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp(MnS)=2.0×10-13,则上述三种难溶物的饱和溶液中,Mn2+浓度由大到小的顺序是Mn(OH)2>MnCO3>MnS(填写化学式).

部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 |
(2)滤渣A的成分除MnO2外,还有Fe(OH)3和Al(OH)3.
(3)MnO2是制造碱性锌锰电池的基本原料,放电时负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2.工业上以石墨为电极电解酸化的MnSO4溶液生产MnO2,阳极的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+,当阴极产生4.48L(标况)气体时,MnO2的理论产量为17.4g.
(4)锰的三种难溶化合物的溶度积:Ksp(MnCO3)=1.8×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp(MnS)=2.0×10-13,则上述三种难溶物的饱和溶液中,Mn2+浓度由大到小的顺序是Mn(OH)2>MnCO3>MnS(填写化学式).
5.某铁矿石样品的主要成分为铁的氧化物,还含有少量SiO2.某化学兴趣小组对该铁矿石中铁元素的价态及含量进行如下探究:
(1)探究铁矿石中铁元素的价态
①提出假设:
假设一:该铁矿石中铁元素的价态为+2;
假设二:该铁矿石中铁元素的价态为+3;
假设三:该铁矿石中铁元素的价态为+2和+3.
②设计实验方案:
为了确定该铁矿石中铁元素的价态,甲同学设计了如下实验方案,请你利用限选试剂帮他完成该探究过程.限选试剂:1mol?L-1H2SO4溶液、3%双氧水溶液、2mol?L-1HNO3溶液、0.01mol?L-1高锰酸钾溶液、1mol?L-1NaOH溶液、0.1mol?L-1KI溶液、0.01mol?L-1KSCN溶液、蒸馏水.
③问题讨论:
乙同学设计了如下实验方案:取少量样品于试管中,滴加适量的2mol?L-1HNO3溶液,加热溶解,得到B溶液,取少量B溶液于试管中,向其中滴加几滴0.01mol?L-1KSCN溶液,溶液变红色,说明该铁矿石中铁元素的价态为+3.你认为此结论错误(填“正确”或“错误”),其理由是稀硝酸具有强氧化性,能将样品中+2价的铁氧化为+3价的铁.
(2)探究铁矿石中铁的含量
将2.25g该铁矿石样品经一系列化学处理,制得铁元素全部为Fe2+的待测液250mL;现利用0.02mol?L-1酸性高锰酸钾溶液对铁矿石中铁元素的含量进行测定.
①取25.00mL待测液于锥形瓶中,用已配制的0.02mol?L-1酸性高锰酸钾溶液进行滴定,判断达到滴定终点的方法是滴加最后一滴酸性高锰酸钾溶液时,溶液由浅黄色突然变为红色,且半分钟内不再变为无色,即达到滴定终点.
②重复此滴定操作2~3次,平均消耗酸性高锰酸钾溶液21.50mL,则该铁矿石中铁元素的质量分数为53.5%.
(1)探究铁矿石中铁元素的价态
①提出假设:
假设一:该铁矿石中铁元素的价态为+2;
假设二:该铁矿石中铁元素的价态为+3;
假设三:该铁矿石中铁元素的价态为+2和+3.
②设计实验方案:
为了确定该铁矿石中铁元素的价态,甲同学设计了如下实验方案,请你利用限选试剂帮他完成该探究过程.限选试剂:1mol?L-1H2SO4溶液、3%双氧水溶液、2mol?L-1HNO3溶液、0.01mol?L-1高锰酸钾溶液、1mol?L-1NaOH溶液、0.1mol?L-1KI溶液、0.01mol?L-1KSCN溶液、蒸馏水.
| 实验步骤 | 预期现象及结论 |
| 步骤1:取少量样品于试管中,滴加适量的1mol?L-1H2SO4溶液,加热溶解,得到A溶液 | |
| 步骤2: | 若高锰酸钾溶液紫红色褪去,则样品中含+2价的铁元素 |
| 步骤3: | 若溶液变红色,则样品中含+3价的铁元素 |
乙同学设计了如下实验方案:取少量样品于试管中,滴加适量的2mol?L-1HNO3溶液,加热溶解,得到B溶液,取少量B溶液于试管中,向其中滴加几滴0.01mol?L-1KSCN溶液,溶液变红色,说明该铁矿石中铁元素的价态为+3.你认为此结论错误(填“正确”或“错误”),其理由是稀硝酸具有强氧化性,能将样品中+2价的铁氧化为+3价的铁.
(2)探究铁矿石中铁的含量
将2.25g该铁矿石样品经一系列化学处理,制得铁元素全部为Fe2+的待测液250mL;现利用0.02mol?L-1酸性高锰酸钾溶液对铁矿石中铁元素的含量进行测定.
①取25.00mL待测液于锥形瓶中,用已配制的0.02mol?L-1酸性高锰酸钾溶液进行滴定,判断达到滴定终点的方法是滴加最后一滴酸性高锰酸钾溶液时,溶液由浅黄色突然变为红色,且半分钟内不再变为无色,即达到滴定终点.
②重复此滴定操作2~3次,平均消耗酸性高锰酸钾溶液21.50mL,则该铁矿石中铁元素的质量分数为53.5%.